抗体药物偶联物(ADC)是一类用于治疗癌症的新兴靶向疗法,旨在将小分子化疗直接递送并杀伤肿瘤细胞,同时保留健康细胞。自2000年吉妥珠单抗奥佐米星成功获批以来,抗体药物偶联物(ADC)已成为癌症靶向治疗的关键类别。ADC主要由三部分构成单克隆抗体、连接子和毒素三部分构成。抗体是决定ADC疗效的关键;连接子决定着ADC药物系统毒性及临床疗效;毒素是决定ADC药物杀伤力大小的关键因素。尽管目前公布的ADC药物中所用毒素种类超过130余种,但处于临床试验或已上市的ADC药物所用毒素只有6-8个。按作用方式可大致分为三类:微管蛋白抑制剂、DNA合成抑制剂和拓扑异构酶抑制剂。其中以微管蛋白抑制剂中的MMAE作为毒素分子的ADC药物获批最多。今天我们重点介绍了MMAE的定义及在ADC中的应用与作用机理。
1、ADC药物中毒素的发展史
在开始介绍MMAE之前,我们先来了解下ADC药物中毒素的发展史。ADC药物的概念最早是由德国诺贝尔奖获得主Paul Ehrlich于1913年提出。但ADC药物开发的开始时间是1975年,因为那个时候杂交瘤技术才开始用于生产单克隆抗体。经过近50年的研发发展,ADC药物经历三次迭代更新。在这三代ADC药物中,所涉及的毒素也各有特点:
第一代ADC药物主要是以传统化疗药物作为毒素,比如甲氨蝶呤、长春花碱和阿霉素等。但由于传统化疗药物对癌细胞的细胞毒性弱、特异性不强,而且不易在靶细胞中蓄积,导致这代ADC的疗效甚至比化药单独用的效果更差。
第二代ADC药物中使用的毒素主要是微管蛋白抑制剂,比如MMAE、MMAF等。这是一类新型高细胞毒性化合物,其癌细胞毒性比第一代ADC中使用的传统化疗药物强100至1000 倍。但值得注意的是,这类毒素作为单一药物用于杀死肿瘤时,往往会产生难以忍受的副作用,所以,它们并没有被批准作为单一药物用于癌症治疗。不过,这类毒素是ADC药物开发中毒素选择的理想型。因为与正常细胞相比,分裂速度更快的肿瘤细胞对微管蛋白抑制剂更敏感。但这类毒素也有一个弊端,就是它们对分裂中的肿瘤细胞杀伤效果优于静态癌细胞。
第三代ADC药物开发过程中,为了避免这一限制,大多数药物选择了可靶向整个细胞周期的DNA损伤剂作为偶联毒素,比如烯二炔、拓扑异构酶I抑制剂和吡咯并苯二氮卓类。DNA损伤剂可以通过双链断裂、烷基化、嵌合和交联破坏DNA结构来杀死肿瘤细胞 [1]。
尽管ADC药物已经迭代了三次,但ADC药物偶联毒素仍然存在临床局限性,比如严重的副作用和耐药性。在目前获批的15款ADC药物中,以MMAE作为毒素分子的ADC药物有5款。
2、什么是MMAE?
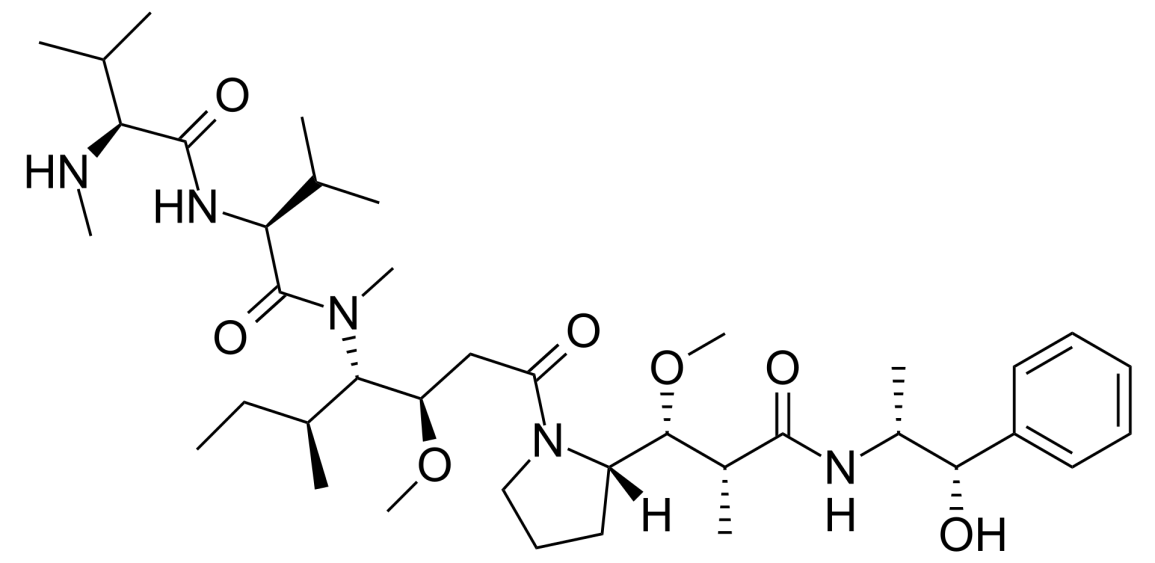
甲基澳瑞他汀E(Monomethyl auristatin E,MMAE)是一种细胞毒素,它可以杀死癌细胞。MMAE是海兔毒素10(Dolastatin 10)的类似物。微管由a-微管蛋白和b-微管蛋白组成,是细胞骨架的主要组成部分。微管蛋白抑制剂是通过破坏肿瘤细胞的细胞骨架结构并干扰有丝分裂来杀死肿瘤细胞。海兔毒素10是从印度洋海兔(Dolabella auricularia)中分离提取的,是一种微管抑制剂,具有极强的细胞毒性。人工合成的海兔毒素10类似物除了MMAE,还有单甲基奥瑞他汀F(MMAF),二者均被广泛用于ADC的载荷成分,即ADC毒素。MMAE 包含四种氨基酸:单甲基缬氨酸 (MeVal)、缬氨酸 (Val)、多莱异亮氨酸 (Dil) 和多拉脯氨酸 (Dap),以及羧基末端胺去甲麻黄碱。在MMAF中,单甲基缬氨酸的C端被苯丙氨酸取代,其细胞活性显着降低。
MMAE实质是去甲基化的奥瑞他汀 E(auristatin E),即N-末端氨基只有一个甲基取代基,而不是像奥瑞他汀 E 本身那样有两个甲基取代基 [2]。MMAE是一种合成抗肿瘤药,其效力比阿霉素强100-1000倍。由于其毒性,MMAE本身不能作为药物使用。但它与单克隆抗体相连后,由于单克隆抗体可识别癌细胞中的特定标记物,可将MMAE引导至特定的癌细胞。
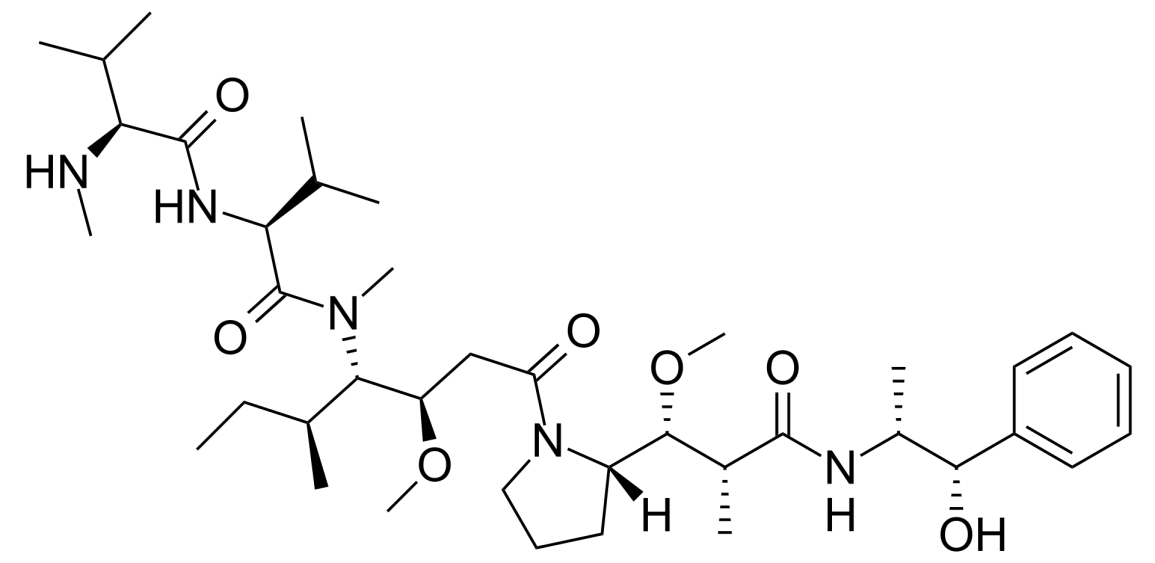
Figure 1. the structure of MMAE (Origin from Wikipedia)
3、MMAE在ADC中的应用及作用机理
如前所述,MMAE作为热门小分子药物广泛用于抗体药物偶联物 (ADC) 开发,用于治疗多种不同的癌症类型,是目前使用最广泛的有效负载。例如,Adcetris、Polivy、padcev 和 vidicizumab 都使用了MMAE。本文中以Adcetris为例对MMAE的作用机理进行阐述。
Adcetris中文名词为维布妥昔单抗,是由日本武田制药和美国西雅图遗传学公司联合开发的一款靶向CD30的抗体偶联药物(ADC)。 Adcetris于2011年获美国FDA批准,用于治疗系统性间变性大细胞淋巴瘤(sALCL)、经典型霍奇金淋巴瘤(cHL)、原发性皮肤间变性大细胞淋巴瘤(pcALCL)或蕈样真菌病(MF)等。Adcetris由抗体、连接子和MMAE三部分组成。抗体部分是针对人CD30的特异性抗体;抗体通过可被蛋白酶水解的连接子与MMAE相连。每个抗体分子上大约有4个MMAE分子,这样使得Adcetris具有高效的靶向作用,在靶细胞内可释放出高浓度的MMAE以发挥药物效应。
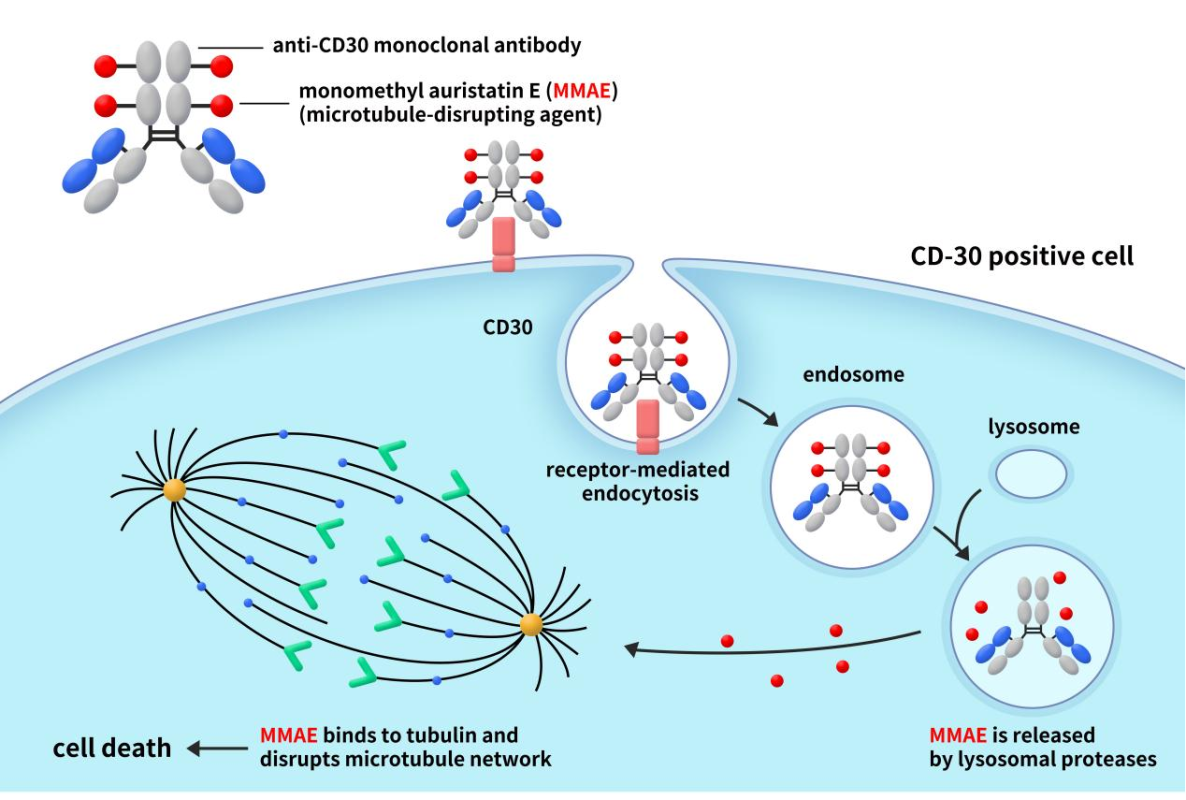
Figure 2. the mechanism of action of Adcetris [3]
如图2所示,当Adcetris抗体部分与肿瘤细胞表面的CD30结合后,CD30-Adcetris复合物会经细胞内吞并作用转运至溶酶体。连接MMAE与单克隆抗体的linker在细胞外液中稳定,但一旦ADC与靶向癌细胞抗原结合并进入癌细胞,则被组织蛋白酶切割并释放出游离的MMAE。游离的MMAE会进一步释放到细胞内部,与细胞内的微管蛋白结合,抑制微管蛋白聚合,并破坏微管网络,从而破环细胞分裂和增殖能力,导致肿瘤细胞停滞在G2/M细胞周期并最终死亡。此外,MMAE还能从CD30阳性淋巴瘤细胞扩散到周围肿瘤微环境中,发挥旁观者效应 [4],进一步增强抗肿瘤作用。这一优势可以有效杀死肿瘤细胞。但它同时也会对健康细胞造成毒性。所以,在以在ADC分子开发中,对生产的ADC进行深入的分析表征以及体内药理学研究是确保药物安全的基础。为了表征ADC的PK特性,通常测量三种分析物:抗体缀合MMAE (AcMMAE)、总抗体和未缀合的MMAE。
4、缔码生物anti-MMAE抗体助力ADC药物研发
由于ADC毒素具有高细胞毒性,ADC有效负载的PK研究对于了解有效负载的行为非常重要 [5]。但由于MMAE 本身具有毒性,不允许在人体中进行此类研究。所以临床前检测MMAE水平(比如测定ADC、抗MMAE中偶联MMAE的浓度)非常重要。缔码生物开发了适合ADC ELISA 测定开发的anti-MMAE抗体,它可用于定量测定测试样品中anti-MMAE-缀合物的水平, 可用于PK检测以及DAR值分析,加速ADC药物的研发进程。
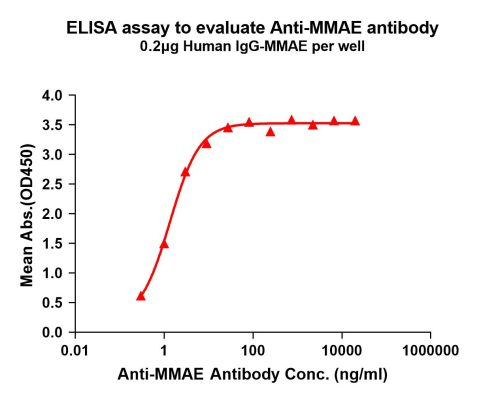
Figure 3. Elisa plates were pre-coated with IgG-MMAE (0.2μg/per well). Serial diluted anti-MMAE monoclonal antibody (DME101004) solutions were added, washed, and incubated with secondary antibody before Elisa reading. From above data, the EC50 for anti-MMAE monoclonal antibody binding with IgG-MMAE is 1.356ng/ml.
- 更多anti-MMAE抗体产品
| 货号 | 产品名称 |
| DME101007 | Anti-MMAE antibody(11C8); Rabbit mAb |
| DME101006 | Anti-MMAE antibody(11B2); Rabbit mAb |
| DME101005 | Anti-MMAE antibody(9C4); Rabbit mAb |
| DME101003 | Anti-MMAE antibody(8B4); Rabbit mAb |
参考文献:
[1] Wang Z, Li H, Gou L, Li W, Wang Y. Antibody-drug conjugates: Recent advances in payloads. Acta Pharm Sin B. 2023 Oct;13(10):4025-4059. doi: 10.1016/j.apsb.2023.06.015. Epub 2023 Jun 30.
[2] Dosio, F.; Brusa, P.; Cattel, L. Immunotoxins and Anticancer Drug Conjugate Assemblies: The Role of the Linkage between Components. Toxins 2011, 3, 848-883.
[3] Graham P Collins, David Bruce, Toby A Eyre. New Therapies in T-cell Lymphoma [J]. Lymphoma and Chronic Lymphocytic Leukemias. 2014, 1(4):1-8.
[4] Kovtun YV, Audette CA, Ye Y, Xie H, Ruberti MF, Phinney SJ, Leece BA, Chittenden T, Blättler WA, Goldmacher VS. Antibody-drug conjugates designed to eradicate tumors with homogeneous and heterogeneous expression of the target antigen. Cancer Res. 2006 Mar 15;66(6):3214-21.
[5] O’Connor O.A., Lue J.K., Sawas A., Amengual J.E., Deng C.C., Kalac M., Falchi L., Marchi E., Turenne I., Lichtenstein R., et al. Brentuximab vedotin plus bendamustine in relapsed or refractory Hodgkin’s lymphoma: an international, multicentre, single-arm, phase 1-2 trial. Lancet Oncol. 2018;19:257–266.