1、稳转细胞株的定义及特点
稳转细胞株,也称为稳定细胞株,指的是通过基因工程手段获得的持续稳定过表达或者干扰特定基因的细胞株。稳定转染(又称稳转)旨在将外来DNA整合到宿主基因组中以便于永久改变细胞的遗传组成。稳转细胞株的主要优势在于它能够在较长的时间内维持基因表达的一致性。基于这个优势,稳转细胞株应用范围广(比如重组蛋白和抗体生产、基因编辑、功能性研究)且经稳转细胞株生产的生物制品批间差小。
2、稳定转染与瞬时转染的区别
与稳定转染相对应的是瞬时转染,什么是瞬时转染?顾名思义,指将外来遗传物质(通常是DNA或RNA)暂时引入宿主细胞,进行短期表达,而不会永久整合到细胞基因组中。
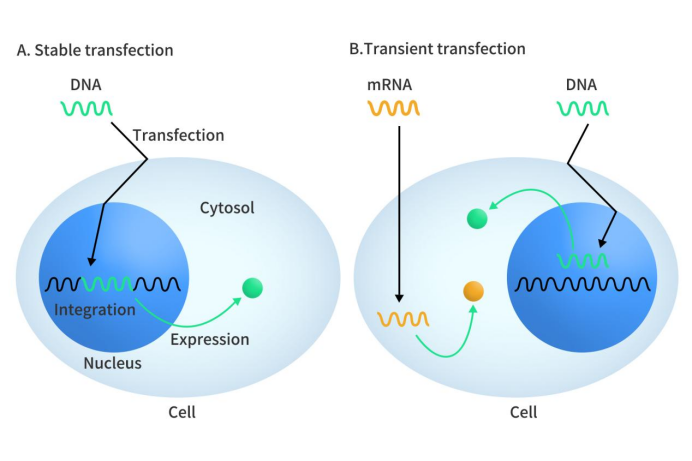
Figure 1. Schematic diagrams of two different transfections [1]
除了外源基因是否整合到宿主细胞这个区别外,稳定转染可实现外源基因的持续表达,而且需要构建细胞系;构建一个稳转细胞株耗时6至12个月是常态;可适用于持续进行且具有稳定改变的研究。与稳定转染不同,瞬时转染中外源基因表达的时间短,通常只有几天,而且无需建立细胞系,耗时短且方便;不过只适用于只需进行临时基因改造即可进行的实验。尽管稳定转染有诸多优点,但在选择是用稳定转染还是瞬时转染时,主要依据还是取决于研究目标的具体要求。
选用稳定转染的情况通常有以下几种:
- 需要长期和持续基因表达或持续蛋白质生产的研究,稳定转染通常是首选途径。因为通过构建稳定株,可以大大降低频繁转染或者病毒包装的成本,这也极大方便实验研究;
- 部分蛋白半衰期极长,瞬时RNA只能干扰表达,却无法去除已表达的目的蛋白,这种情况通过构建稳转细胞株可以实现更好的基因干扰效果;
- 需要用诱导表达系统的,主要是一些致死基因或者是需要时空表达的;
- 若是需要用细胞做动物实验的,比如裸鼠成瘤等,往往需要构建成稳转株。
选择瞬时转染的情况有:
- 短期实验或需要快速产生蛋白质且不需要持久的基因改变的情况。因为这种方法灵活且快速,可最大限度地降低意外基因组整合的风险,且无需建立稳定的细胞系。
- 针对于那些开发合适的稳转细胞株存在困难的项目,瞬时转染通常也是临床试验中大规模批量生产慢病毒载体的首选方法。
那目前常用于构建稳转细胞株的方法又有哪些?
3、构建稳转细胞株的方法
目前稳转细胞系的构建方法主要包括慢病毒介导、转座子介导、CRISPR敲入及质粒筛选四种方法。其中,质粒筛选是最原始的细胞系构建方案,操作上只需要把目的质粒成功转染到细胞内,然后使用对应抗性长期筛选,有一定的概率获得稳转细胞株,但效率低且不稳定,尽管成本低,但已不是首选。由于慢病毒几乎可以感染所有类型的细胞,并且可以将遗传物质整合到宿主细胞基因组中,进行长时间的稳定表达,而且介导效率高,所以慢病毒介导方法是当前稳转细胞株构建的主流方法。
4、慢病毒介导稳赚细胞株构建过程
慢病毒介导的稳转细胞株构建主要分为三大步:慢病毒表达载体构建、慢病毒包装及稳转细胞株构建。
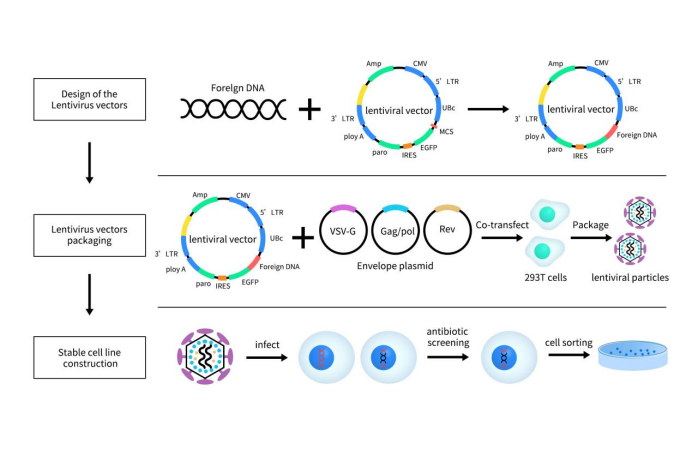
Figure 2. Stable Cell Lines generation by lentivirus
慢病毒表达载体构建主要是将外源基因构建到慢病毒载体中生成重组慢病毒载体,这通常涉及目的基因的确定及表达载体的选择。关于表达载体的选择,这个需要根据自己的实验目的进行选择。通常可根据载体抗性、启动子类型、可溶和表达荧光蛋白、是否需要筛选稳转株等选择合适的载体。
慢病毒包装主要是指将重组慢病毒载体与包装质粒(如rev、gag/pol、vsv-g等)共转染到宿主细胞中,用来产生具有感染能力的慢病毒颗粒。为了能高效感染目的细胞,在这步,我们通常会对病毒进行浓缩及滴度测定。关于病毒浓缩,通常是在转染后48-72小时后收集含有病毒颗粒的培养基,通过超速离心沉淀法、PEG8000浓缩法等方法进行浓缩,以提高病毒滴度。
稳转细胞株构建这一环节包括病毒感染靶细胞、筛选稳转细胞、单克隆培养、扩增与鉴定及功能研究。其中,最重要的是病毒感染靶细胞和筛选稳转细胞。病毒感染靶细胞是指将上一步中浓缩的病毒颗粒与靶细胞共培养,使病毒整合到宿主细胞基因组中,感染效率可通过观察绿色荧光蛋白(GFP)等报告基因的表达来评估。注意,在病毒感染靶细胞时,由于慢病毒对不同种属、不同组织来源细胞的感染性差别很大,需要针对不同类型的细胞计算感染复数(MOI),即感染时病毒和细胞数量的比值。筛选稳转细胞通常是在病毒感染靶细胞后,通过抗生素筛选(如嘌呤霉素、新霉素等)或其他筛选标记,筛选出稳定表达外源基因的细胞克隆。
5、稳转细胞株在抗体药物发现中的应用
如前所述,稳转细胞株的主要特点是将目标基因整合到其基因组中,从而实现持续表达,生产的生物制品批间差小。基于这个优势,稳转细胞株可广泛应用于药物发现的多个阶段,包括靶点识别与验证、筛选与检测开发和重组蛋白抗体生产。在靶点识别与验证阶段,稳转细胞株通过在受控环境中稳定表达靶点蛋白,可用于识别和验证潜在药物靶点;在筛选与检测开发阶段,稳转细胞株可用于识别潜在药物候选分子,并开发可靠的检测方法以测试药物的有效性;在重组蛋白抗体生产阶段,利用稳转细胞株,可确保蛋白抗体生产的一致性和高效性,而且稳转细胞株也适合大规模生产。由于稳转细胞株都是哺乳动物细胞,可对生产的重组蛋白抗体进行必要的修饰,模拟人类特有的糖基化修饰,这对治疗效果至关重要。目前,已有多家生物制药公司利用稳转细胞株生产单克隆抗体,如曲妥珠单抗(Herceptin)和利妥昔单抗(Rituxan),这些药物被广泛用于治疗疾病。
除了抗药物发现,稳转细胞株在CAR-T细胞疗法发展进程中也功不可没。通过生产嵌合抗原受体(CAR),这些CAR被工程化导入T细胞,增强其对癌细胞的靶向和杀伤能力。
6、缔码130+现货稳转细胞株,助力药物研发
缔码生物是一家专注于可成药靶点临床前研发产品和服务的生物技术公司。缔码最近推出了130+新型稳转细胞株,这些细胞株能够在常用的细胞系(如K562、293T、CHO-S和Jurkat等)中稳定表达药物靶点蛋白(如GPRC5D、B7H4、CLDN6、Trop2和PD-L1等)。这些新研究工具为药物发现提供了强大的支持,能够加速靶点验证、抗体筛选及其他药物开发流程。通过使用我们的稳转细胞株,研究人员可以大幅提高实验的一致性和生产效率,帮助推动新药的快速开发。
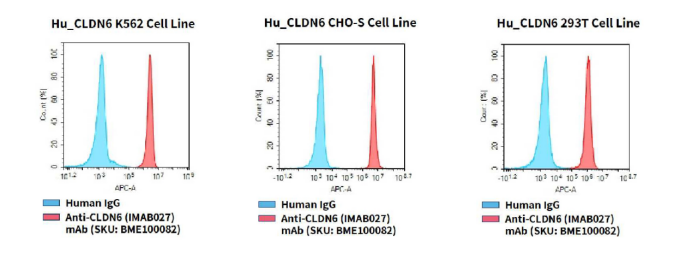
- 部分细胞株验证数据
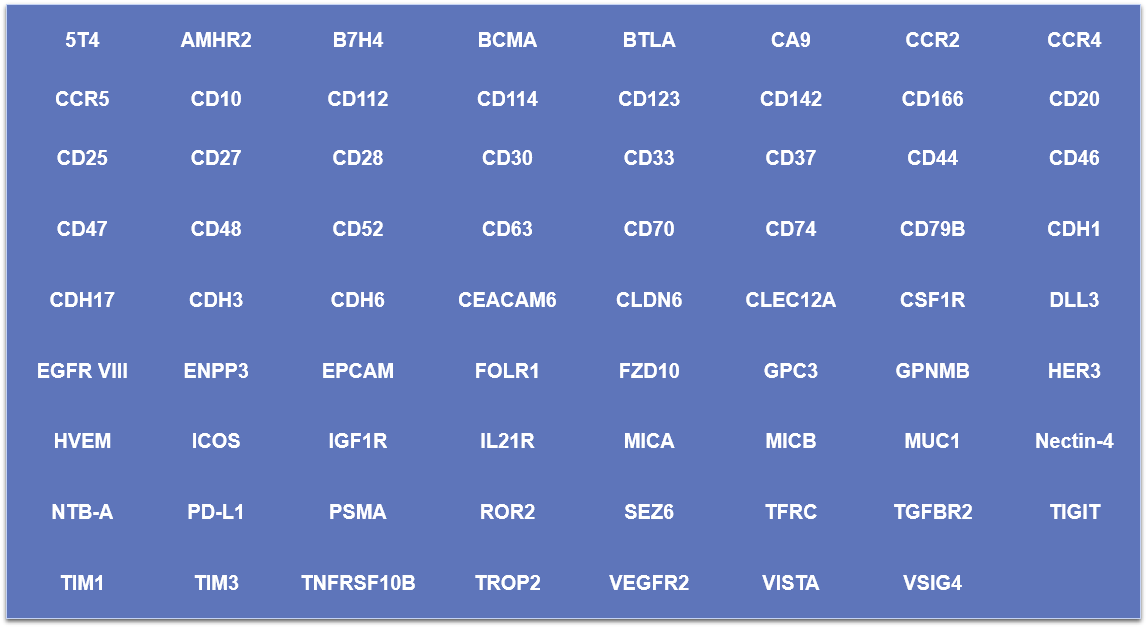
- 稳转细胞株热门现货靶点
参考文献:
[1] Kim, T. K., & Eberwine, J. H. (2010). Mammalian cell transfection: the present and the future. Analytical and bioanalytical chemistry, 397(8), 3173–3178.

