在刚过去的2024 ASCO年会上,多禧生物公布了其STEAP1 ADC(DXC008)的临床前数据。这是一款STEAP1/PSMA双抗ADC,对STEAP1有高亲和力,而且对PSMA也有中等亲和力。临床前数据表明:在高和中STEAP1和PSMA双表达的异种移植模型中,1mpk单次给药下即显示出非常好的持久性抗肿瘤反应。但真正让STEAP1靶点再次引起关注的并不是多禧的DXC008,而是安进的AMG 509。AMG 509是一款靶向STEAP1的人源化的TCE分子,在一期转移性去势耐受性癌症(mCRPC)上的亮眼成绩,单药PSA50为49%,客观有效率(ORR)为24%;毒性稍高但是整体安全性算良好。那STEAP1究竟是怎样一个靶点?目前相关临床药物布局又是如何?
1、STEAP1的结构与功能
六跨膜前列腺上皮抗原1(STEAP1),又称为PRSS2或STEA1,属于前列腺六跨膜上皮抗原(STEAP)家族,该家族还包含成员STEAP1B、STEAP2、STEAP3、STEAP4。其中,STEAP1B是STEAP1的截短同源物,是一个四次跨膜蛋白。STEAP1-4是金属蛋白酶,在铁和铜稳态中发挥重要作用 [1]。STEAP1基因位于染色体 7q21.13上,该基因由5个外显子和4个内含子组成,长度为10.4kb。STEAP1基因转录起始于1.4和4.0 Kb的mRNA 转录体,但只有1.4 Kb mRNA编码STEAP1蛋白。STEAP1蛋白含有339个氨基酸,分子量为39.72KDa,是第一个报道的STEAP蛋白。STEAP1蛋白有六个跨膜结构域,其N端和C端均位于细胞质侧 [2]。其中,C端与STEAP2-4一样,均含有含b型血红素的FRE结构域。但与STEAP2-4不同的是,STEAP1的N端缺乏NADPH结合FNO结构域,因此,STEAP1不能独立表现出 Fe 3+或 Cu 2+还原酶活性[3]。
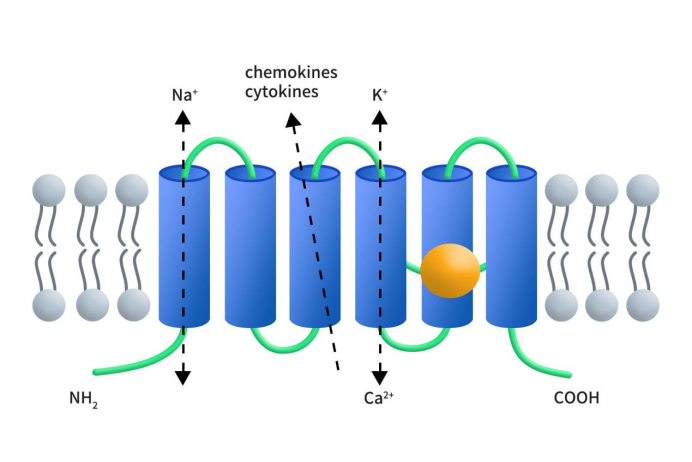
Figure 1. The structure of STEAP1 [2]
STEAP家族蛋白的结构相似,从细胞定位角度看,STEAP家族蛋白均位于细胞膜和细胞质中。位于质膜表面的STEAP1~4蛋白均具有6个潜在的跨膜区,以及一个胞内的亲水性氨基和羧基末端,提示STEAP蛋白可能作为通道或转运体发挥作用;STEAP1和STEAP2的蛋白质结构在膜上含有至少一个血红素基团,这可能与铁和铜的吸收有关 [5]。如前所述,STEAP1由于缺少NADPH结合FNO结构域,所以不能还原金属,但有研究表明,STEAP1可通过与STEAP4的细胞内NADPH结合结构域融合而表现出细胞铁还原酶活性[4]。STEAP1的二级结构与其位于前列腺分泌上皮细胞间连接处的位置有关,表明其在细胞间通讯中发挥作用,可调节小分子和离子(如 Na+、Ca2+ 和K+)的运输,并释放可溶性细胞因子和趋化因子。
2、STEAP1与肿瘤
相对于正常前列腺组织,STEAP1在恶性前列腺组织中过表达。目前对STEAP1的研究主要集中在前列腺癌中,STEAP1过表达促进前列腺肿瘤生长,而STEAP1敲低则抑制前列腺肿瘤生长。除了前列腺癌,在其他肿瘤组织中也观察到上调的STEAP1表达,包括肾细胞癌、膀胱癌、尤文氏肉瘤、乳腺癌、结直肠癌 (CRC)、胃癌、卵巢癌和肺癌。尽管关于STEAP1在肿瘤中的具体作用机制还需进一步研究,但已有少量研究揭露了部分机制。在前列腺癌中,STEAP1作为细胞表面膜蛋白,是肿瘤细胞与邻近肿瘤基质细胞之间细胞间通讯所必需的,以促进肿瘤生长[6]。在雄激素依赖性前列腺癌中,敲低STEAP1可抑制细胞生长并以DHT非依赖的方式诱导LNCaP前列腺癌细胞凋亡[7]。在肺腺癌中,敲低STEAP1可显著抑制肺腺癌细胞的增殖和迁移,STEAP1可通过JAK2 / STAT3信号通路调节上皮-间质转化 (EMT)[8]。在结直肠癌(CRC)中,高STEAP1转录水平可导致ROS生成减少,从而阻止CRC 细胞通过NRF2通路凋亡[9]。在肝癌中,敲低STEAP1可抑制肝癌细胞中c-Myc的表达,从而使癌细胞停滞在G1期并抑制细胞增殖[10]。
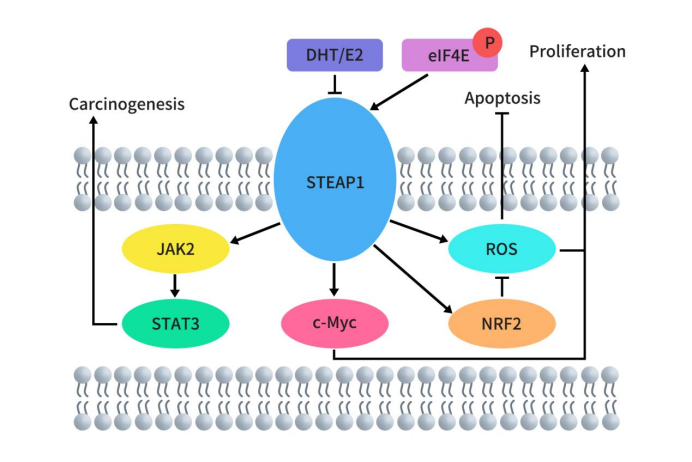
Figure 2. Molecular mechanisms of STEAP1 in cancer [5]
3、STEAP1靶向疗法临床研究进展
不完全统计,目前处于临床阶段的STEAP1药物共4项,涉及抗体、CAR-T和ADC等多种疗法,最高的临床研究进展为临床II期。
- 89Zr-DFO-MSTP2109A
89Zr-DFO-MSTP2109A是由Genentech, Inc.和Memorial Sloan Kettering Cancer Center联合开发的靶向STEAP1的放射性标记抗体。目前89Zr-DFO-MSTP2109A已完成临床1/2期试验(NCT01774071),但具体结果尚未公布。之前的研究表明,89Zr-DFO-MSTP2109A患者耐受良好,能清楚定位骨和软组织转移性去势抵抗性前列腺癌(mCRPC)病灶。
- STEAP1 CAR-T Cell Therapy
STEAP1 CAR-T Cell Therapy是由PromiCell Therapeutics Inc和弗莱德哈钦森癌症研究中心联合开发的STEAP1 CAR-T细胞疗法。STEAP1 CAR-T是经过STEAP1抗原改造的CAR-T细胞,可以更好地靶向前列腺肿瘤细胞。目前正在临床联合恩杂鲁胺(Enzalutamide)治疗转移性去势抵抗性前列腺癌患者(NCT06236139)。这是一项I/II期临床试验,旨在测试恩杂鲁胺联合STEAP1 CAR-T细胞疗法在治疗前列腺癌患者中的安全性和有效性。该项临床试验于2024 年2月1日首次发布,目前尚未开始招募。
- AMG-509
AMG-509,也称为xaluritamig,是安进与百济共同研发的一款可同时靶向STEAP1和CD3的双特异性T细胞结合器,可与人、灵长类动物的STEAP1抗原和T细胞表面的CD3受体结合。在结构设计上,安进采用Xencor公司的Xmab 2+1非对称技术,并且延长了这一蛋白的半衰期。如下图所示,AMG-509包括两个相同的人源化抗STEAP1 Fab结构域和一个抗CD3 scFv结构域,其中抗CD3 scFv结构域与一端的STEAP1 Fab结构域偶联。2023年10月20日公布的治疗前列腺癌的临床前数据显示,AMG 509 在体外介导前列腺癌细胞系的强效T 细胞依赖性细胞毒性,并在体内促进前列腺癌异种移植和同源小鼠模型中的肿瘤消退 [11]。目前AMG-509目前处于临床I期。
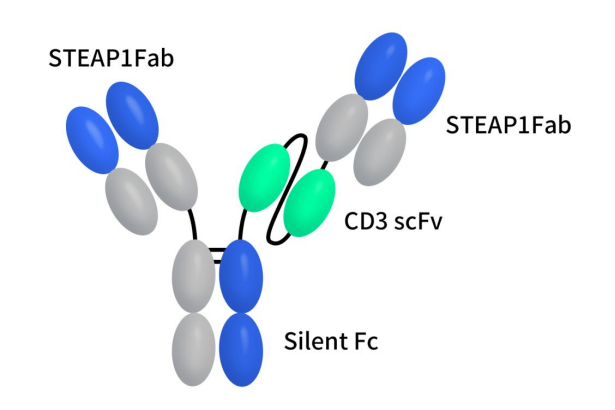
Figure 3. The structure of AMG-509
- ABBV-969
ABBV-969是艾伯维开发的一款PSMA/STEAP1双抗ADC,采用拓扑异构酶作为payload,目前正在针对去势难治性前列腺癌患者启动一期临床试验NCT06318273。该临床预计将从2024年3月开始,计划入组人数120人。
4、缔码STEAP1相关产品助力STEAP1生物药研发
缔码生物科技有限公司是一家专注于可成药靶点临床前研发产品和服务的生物技术公司。公司计划在未来的3-5年完成所有可成药靶点的预制先导抗体分子的制备,让药企跨过单抗平台建立和先导抗体分子筛选的门槛,有更多的时间聚焦于药靶的生物学机制和可成药性研究,从而更快地推进临床管线。缔码现可提供STEAP1靶点全系列产品与服务。产品包括活性蛋白和参照抗体;服务涵盖多种属蛋白抗体定制服务、抗体人源化和亲和力成熟服务。
| 产品类型 | 产品货号 | 产品名称 |
| 全长膜蛋白 | FLP100070 | Human STEAP1 full length protein-synthetic nanodisc |
| ECD蛋白 | PME101530 | Human STEAP1 Protein, hFc Tag |
| 参照抗体 | BME100208 | Anti-STEAP1(xaluritamig without CD3 biosimilar) mAb |
| BME100188 | Anti-STEAP1(Vandortuzumab biosimilar) mAb | |
| 生物素标记抗体 | BME100208B | Biotinylated Anti-STEAP1(xaluritamig without CD3 biosimilar) mAb |
| BME100188B | Biotinylated Anti-STEAP1(Vandortuzumab biosimilar) mAb |
参考文献:
[1]Ohgami R.S., Campagna D.R., McDonald A., et al. The Steap proteins are metalloreductases. Blood. 2006;108:1388–1394.
[2]Barroca-Ferreira J, Pais JP, Santos MM, et al. Targeting STEAP1 Protein in Human Cancer: Current Trends and Future Challenges. Curr Cancer Drug Targets. 2018;18(3):222-230.
[3]Xu M, Evans L, Bizzaro CL, et al. STEAP1-4 (Six-Transmembrane Epithelial Antigen of the Prostate 1-4) and Their Clinical Implications for Prostate Cancer. Cancers (Basel). 2022 Aug 20;14(16):4034.
[4]Oosterheert W, Gros P. Cryo-electron microscopy structure and potential enzymatic function of human six-transmembrane epithelial antigen of the prostate 1 (STEAP1). J Biol Chem. 2020 Jul 10;295(28):9502-9512.
[5]Chen WJ, Wu HT, Li CL, et al. Regulatory Roles of Six-Transmembrane Epithelial Antigen of the Prostate Family Members in the Occurrence and Development of Malignant Tumors. Front Cell Dev Biol. 2021 Oct 29;9:752426.
[6]Yamamoto T, Tamura Y, Kobayashi J, et al. Six-transmembrane epithelial antigen of the prostate-1 plays a role for in vivo tumor growth via intercellular communication. Exp Cell Res. 2013 Oct 15;319(17):2617-26.
[7]Gomes IM, Rocha SM, Gaspar C, et al. Knockdown of STEAP1 inhibits cell growth and induces apoptosis in LNCaP prostate cancer cells counteracting the effect of androgens. Med Oncol. 2018 Feb 20;35(3):40.
[8]Huo SF, Shang WL, Yu M, et al. STEAP1 facilitates metastasis and epithelial-mesenchymal transition of lung adenocarcinoma via the JAK2/STAT3 signaling pathway. Biosci Rep. 2020 Jun 26;40(6):BSR20193169.
[9]Nakamura H, Takada K, Arihara Y, et al. Six-transmembrane epithelial antigen of the prostate 1 protects against increased oxidative stress via a nuclear erythroid 2-related factor pathway in colorectal cancer. Cancer Gene Ther. 2019 Sep;26(9-10):313-322.
[10]Iijima K, Nakamura H, Takada K, et al. Six-transmembrane epithelial antigen of the prostate 1 accelerates cell proliferation by targeting c-Myc in liver cancer cells. Oncol Lett. 2021 Jul;22(1):546. doi: 10.3892/ol.2021.12807.
Nolan-Stevaux O, Li C, Liang L, et al. AMG 509 (Xaluritamig), an Anti-STEAP1 XmAb 2+1 T-cell Redirecting Immune Therapy with Avidity-Dependent Activity against Prostate Cancer. Cancer Discov. 2024 Jan 12;14(1):90-103.
