2024年,核药赛道的交易让人目不暇接……
3月,AstraZeneca斥资24亿美元收购专注于开发新一代放射性偶联药物(RDC)的生物制药公司Fusion Pharmaceuticals。4月,Novartis投入近27.1亿美元,与PeptiDream达成合作协议,共同开发多款大环态靶向偶联核药。5月,Novartis又以10亿美元的预付款收购Mariana Oncology,从而获得Mariana Oncology的创新放射性药物管线和平台。同月,Eli Lilly投入11亿美金与Aktis Oncology达成多靶点研发合作协议,利用Aktis Oncology的新型迷你蛋白技术平台开发抗癌放射性药物。6月,Eli Lilly又与Radionetics达成合作,引进其小分子GPCR靶向核药技术。同时,Eli Lilly获得10亿美元收购Radionetics的排他权。9月,Sanofi投入3.56亿美元与放射性制药公司RadioMedix和OranoMed达成了针对AlphaMedix的授权许可的协议……
关于各大药企巨头对核药布局的新闻还在不断更新,核药赛道似乎变成了药企大佬的必争之地,那核药究竟是什么?目前热门的核药靶点及针对的适应症又有哪些?
1、核药简介
核药也称为放射性药物或核素偶联药物,是指含有放射性同位素用于医学诊断和治疗的一类特殊药物。根据用途,核药可分为诊断用核药和治疗用核药。诊断用核药是利用放射性同位素进行医学诊断,主要包括脏器显像用和功能测定用两类药物。诊断用核药可结合伽马照相机(如PET或SPECT),从分子水平上研究病变组织功能、生化代谢和基因异常表达变化等,从而实现生理病理过程的快速、无损及实时成像。治疗用核药是是指患者通过口服或注射放射性药物能够高度选择性浓集在病变组织,通过其载荷放射性同位素在衰变过程中释放的各种射线杀伤肿瘤组织。
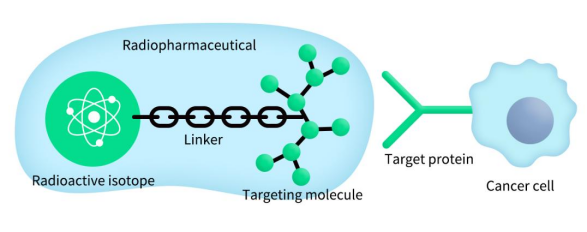
Figure 1. The general structure of radiopharmaceuticals
近年来前列腺特异性膜抗原(PSMA)、成纤维细胞激活蛋白(FAP)、人表皮生长因子受体2(HER2)等新靶点在放射治疗技术(RLT)中的应用,加速了治疗用核药的发展。那究竟是哪些靶点在核药赛道上炙手可热?目前相关药物的研究进展又是如何?
2、“火热”的核药靶点
不完全统计,全球核药药物共有801款,其中受监管批准上市的药物有20种;临床1期和临床2期的药物数量合计达到149种,这表明这个赛道具有较高的可行性;无进展、暂停及终止的药物数量共计有204款;另外,还有289种药物处于临床前阶段,这也意味着制药公司依然在不断地推动新的药物研发。就靶点而言,当前全球药物研发主要集中在PSMA、FAP和HER2等靶点,其中PSMA有26个药物处于临床各阶段研发中。PSMA和FAP的药物研发较为成熟,而且已有部分药物获得批准上市。与之相比,针对SSTR、SSTR2和PDL1等靶点的药物研发数量相对较少,且大部分仍处于临床前或早期阶段。这里重点罗列了热门靶点的临床阶段药物研究进展。
2.1 PSMA
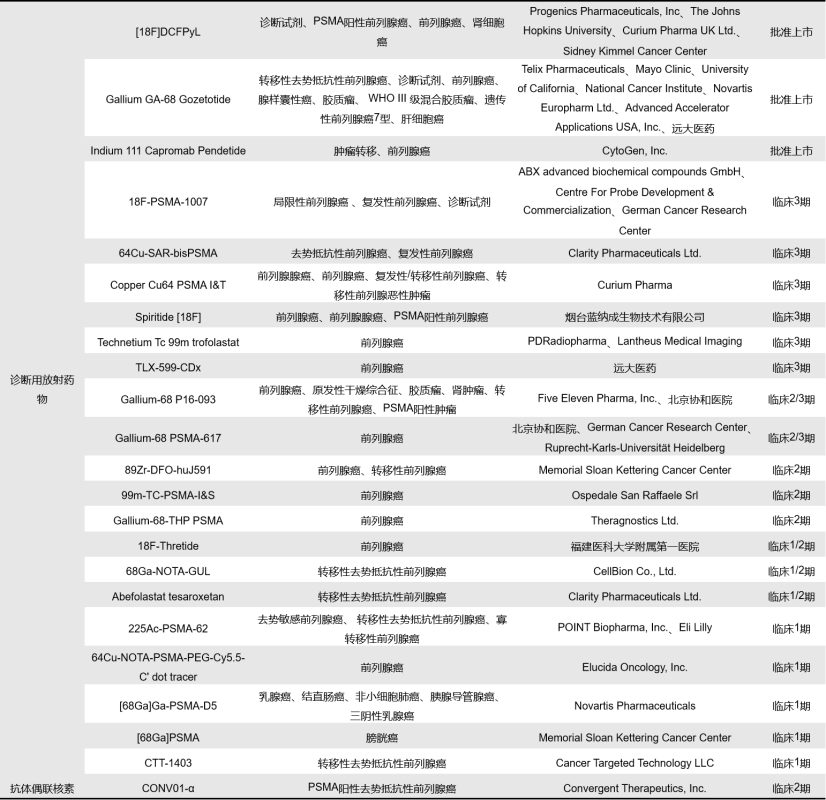
PSMA,也称为谷氨酸羧基肽酶II(GCPII),是一种跨膜糖蛋白酶,存在于细胞表面,具有羧肽酶和叶酸水解酶的活性。PSMA在正常前列腺组织和非前列腺组织中的表达水平极低,但在前列腺癌组织中的表达量是正常组织的100-1000倍。因此,PSMA成为了前列腺癌及其转移组织的影像诊断和靶向放射性核素治疗以及免疫治疗的靶标。目前全球针对PSMA靶点的核药共计有90款,其中处于临床阶段的有43款,已批准上市的有4款。在临床阶段及已上市的药物中,有26款为治疗用放射药物,22款为诊断用放射药物。
治疗用放射药物以诺华的Lutetium (177 Lu) Vipivotide Tetraxetan为代表,该药于2022年3月在美国获批用于治疗PSMA阳性的转移性去势抵抗性前列腺癌(mCRPC),同年 12月在欧盟获批。Lu 177 vipivotide tetraxetan的活性部分是放射性核素镥-177,它与PSMA结合的部分相连。Lu 177 vipivotide tetraxetan与表达PSMA的细胞结合后,镥-177的 β-负辐射会将辐射传递到表达PSMA的细胞以及周围细胞,并诱导DNA损伤,从而导致细胞死亡。诊断用放射药物以CytoGen的Indium 111 Capromab Pendetide为代表,该药于1996年10月在美国获批,是第一个商业化的抗PSMA抗体。不过该抗体只能结合PSMA的细胞内表位。

2.2 FAP
FAP是一种丝氨酸寡肽酶,大多在发育过程中表达,很少在健康的成人组织中表达。然而,在病理组织(包括癌症,纤维化,关节炎,伤口或发炎)重塑部位,尤其是在成纤维细胞上,FAP高度上调。更多关于FAP背景阅读>>
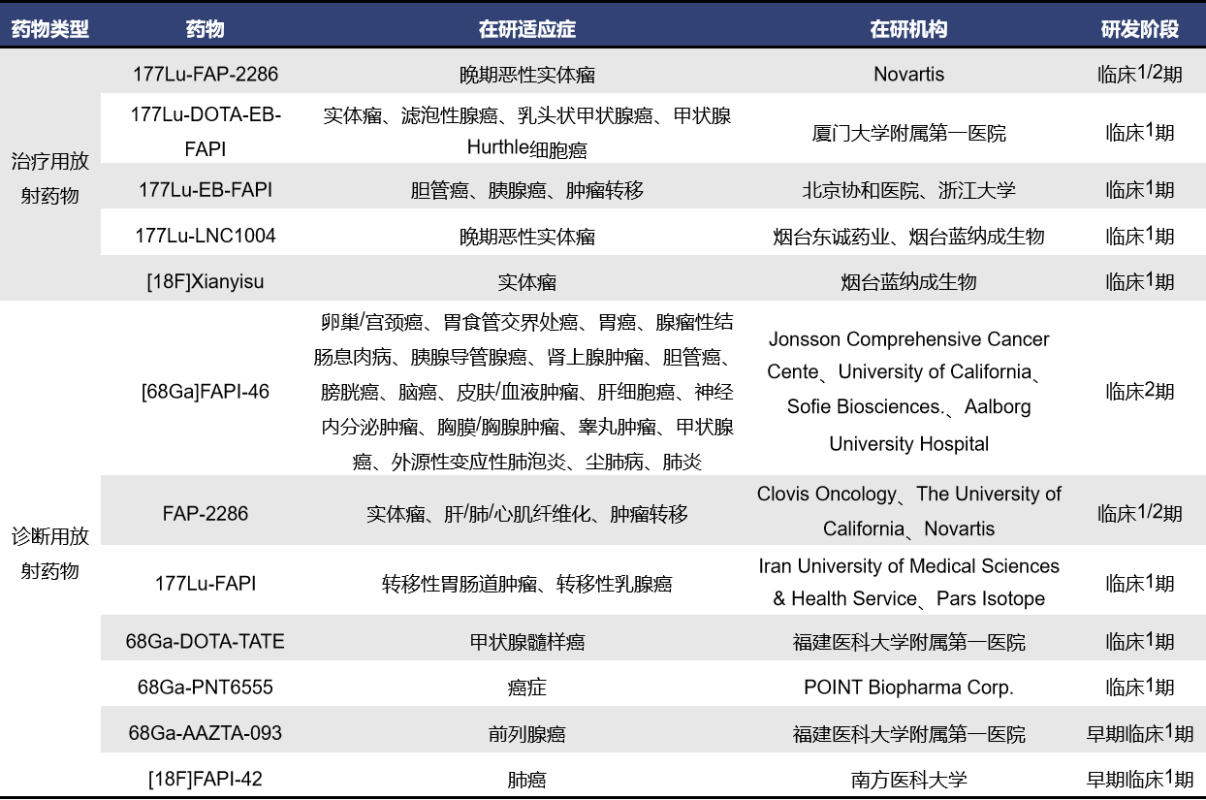
目前全球针对FAP靶点的核药共计有44款,其中处于临床阶段的有12款,临床前的有近28款。在临床阶段的药物中,有5款为治疗用放射药物,7款为诊断用放射药物。
治疗用放射药物以诺华的177Lu-FAP-2286(Clovis Oncology原研)为代表。177Lu-FAP-2286由Clovis Oncology原研,该公司于2022年底被诺华收购。177Lu-FAP-2286是首个肽靶向放射性核素疗法,由一种与FAP结合的靶向肽和一个可附着放射性同位素以供成像和治疗用途的位点构成,目前最高研发阶段为临床1/2期(NCT04939610)。诊断用放射药以[68Ga]FAPI-46为代表。
2.3 HER2
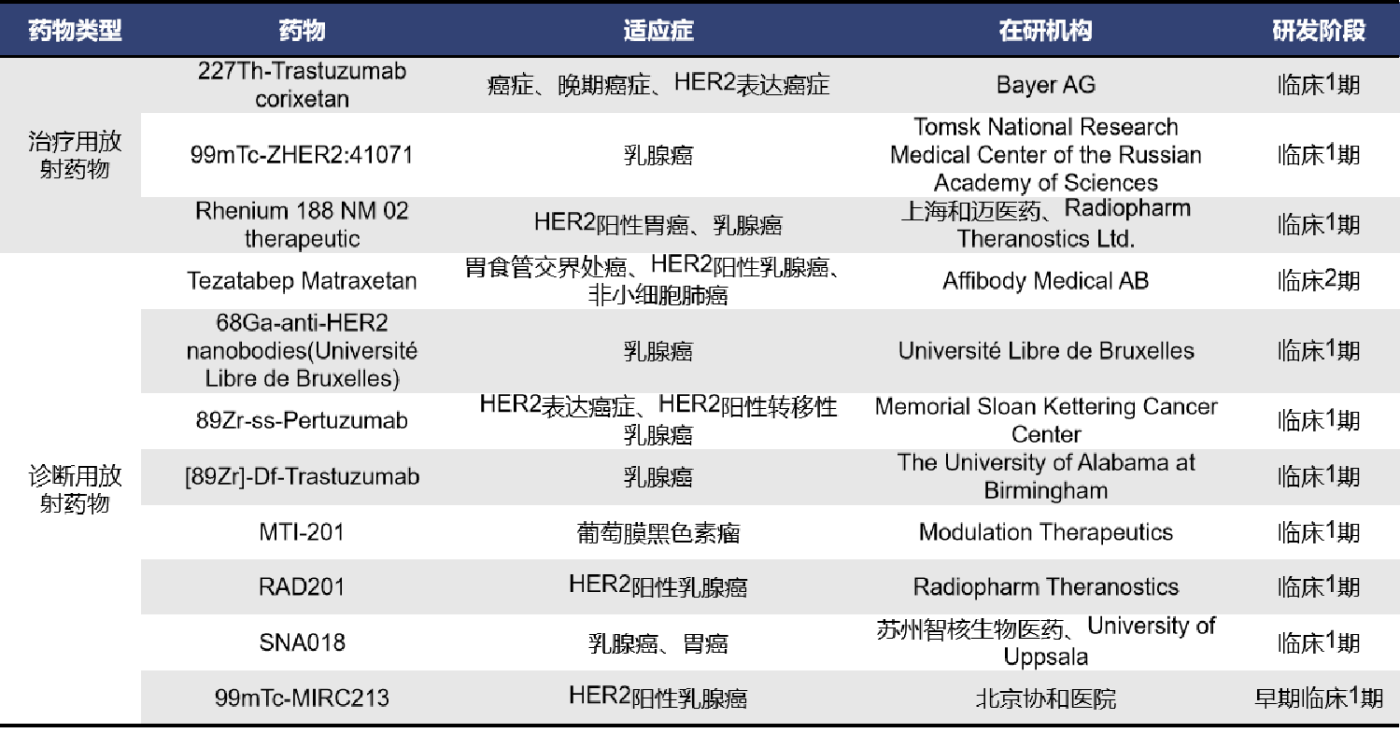
HER2是一种由ERBB2基因编码的酪氨酸激酶受体膜糖蛋白,和EGFR、HER3及HER4一样,都是表皮生长因子受体家族成员。HER2表达异常是恶性肿瘤中最常见的一种现象之一,尤其是在乳腺癌中非常普遍。目前全球针对HER2靶点的核药共计有40款,其中处于临床阶段的有11款,临床前的有近15款。在临床阶段的药物中,有3款为治疗用放射药物,8款为诊断用放射药物。
2.4 SSTR与SSTR2
生长抑素的受体 (SSTR)属于G蛋白偶联受体(GPCR)家族,迄今为止,研究人员已经克隆并鉴定了五种SSTR亚型,分别为SSTR1、SSTR2、SSTR3、SSTR4和SSTR5。SSTR可以在多种正常组织表达,同时也在多种肿瘤组织中高表达。研究发现,来源于不同组织的肿瘤细胞均可以高表达多种SSTR,其中以SSTR2的表达最丰富。目前全球针对SSTR和SSTR2的核药分别有23款,共计是46款,其中批准上市的有5款,处于上市申请阶段的有1款,处于临床阶段的有14款,还有8款处于临床前阶段。
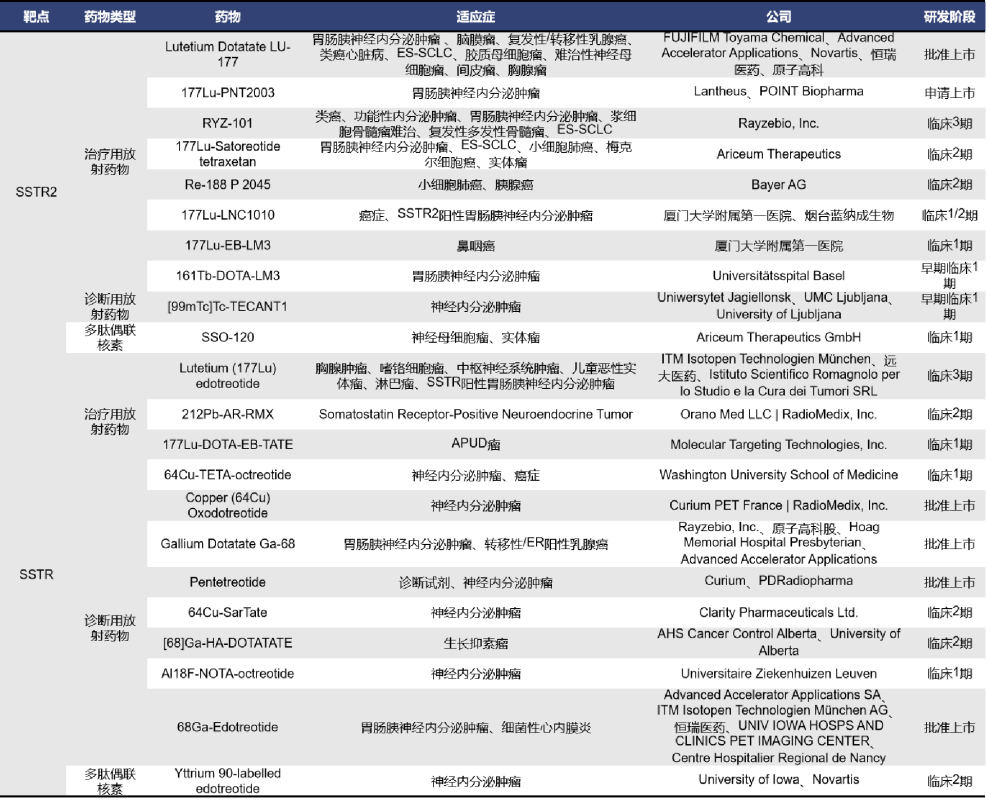
2.5 PDL1
程序性死亡配体1(PDL1),也称为B7H1或CD274,可在癌细胞的表面高表达。它能T细胞结合,令T细胞产生“错觉”,认为癌细胞是“无害的”,同时使得T细胞的活性降低,癌细胞获得自救。目前全球针对PDL1的核药有22款,其中临床阶段的有7款,有12款处于临床前阶段。
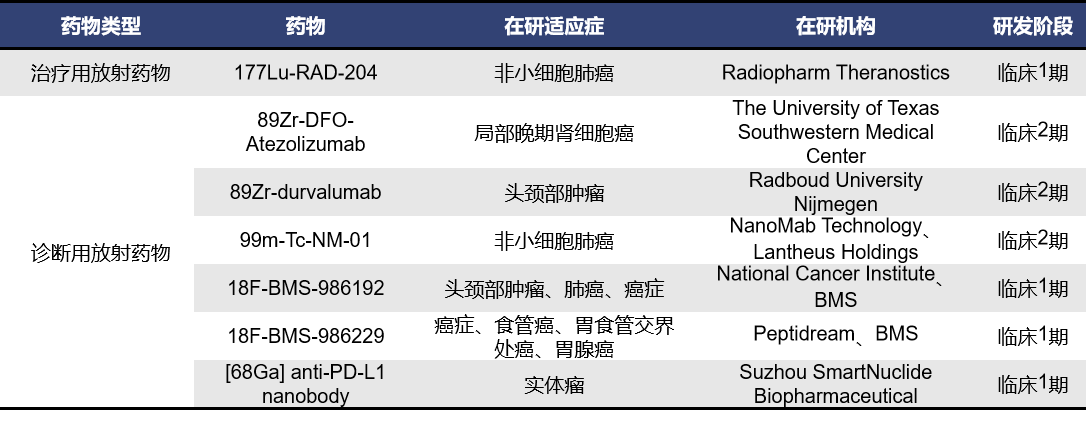
2.6 CAIX
碳酸酐酶IX(CAIX),也称为CA9,是一种在乏氧肿瘤细胞表面特异性过表达的跨膜蛋白,具有调节肿瘤细胞内外酸碱度的功能,与肿瘤增殖、侵袭和转移息息相关。因此,CAIX是一个很有潜力的肿瘤成像和治疗靶点。目前全球针对CAIX的核药有16款,其中有1款正在申请上市,有5款处于临床阶段,有2款处于临床前阶段。
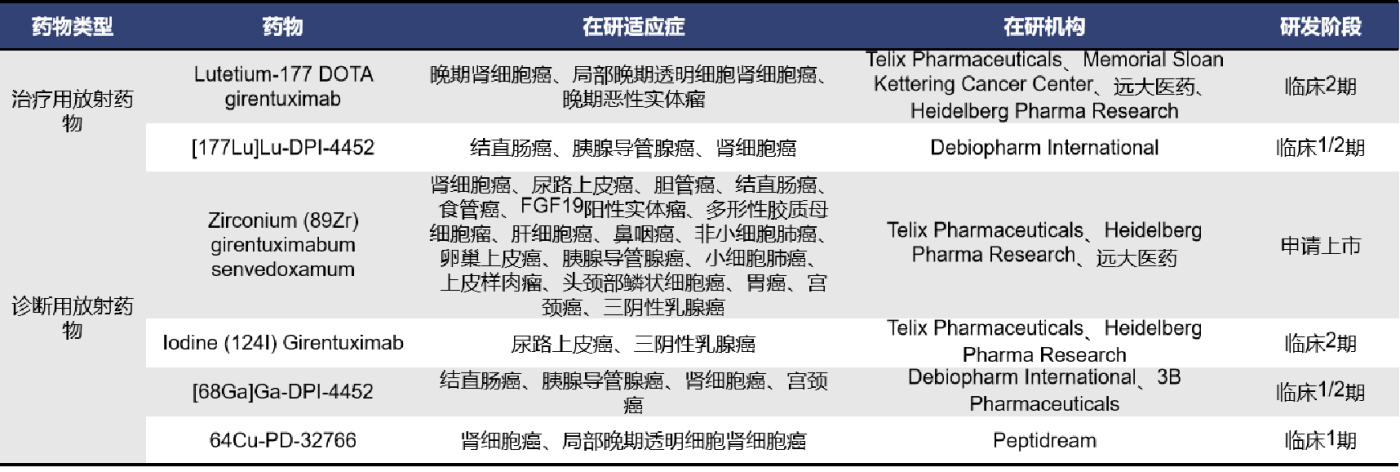
除了以上靶点,也有一批老的肿瘤靶点也加入了核药,比如EGFR、GRPR、MUC1、CD38、CD20、GLP1R、HER3和TROP2等,其中已进入临床阶段药物数量最多的靶点是GRPR,其余靶点核药多处于临床前。
3、缔码现货先导分子助力核药研发
缔码生物科技有限公司是一家专注于可成药靶点临床前研发产品和服务的生物技术公司。针对特定靶点,缔码生物除了可提供靶点相关重组蛋白和抗体产品之外,还可针对性的提供多种属蛋白抗体定制服务、抗体人源化和亲和力成熟服务。此外,为加速ADC药物的开发,缔码还制备了靶点单B细胞种子库,最快28天可获得先导抗体分子;同时,针对热门靶点,我们目前已筛选出多个相关靶点的先导分子,并针对性的验证了人猴蛋白交叉反应,客户第二天可以拿到分子进行功能评估验证。更多先导分子靶点可以参考我们的先导分子手册>>
2024年9月,暨南大学Lu Wang团队在European Journal of Nuclear Medicine and Molecular Imaging杂志上发表了一篇题为“Discovery of a highly specifc radiolabeled antibody targeting B‑cell maturation antigen: Applications in PET imaging of multiple myeloma”研究。缔码生物的BCMA先导分子很荣幸参与了这项研究,点击这里查看研究详情>>
