叶酸受体α(FRα)因其在多种肿瘤或癌组织和正常组织中差异化表达的特点,被认为是一个理想的成药靶点。之前也有药企开展FRα靶向小分子偶联药物或单抗药物的开发,如卫材的人源化单抗farletuzumab,和Endocyte的小分子偶联药物Vintafolide,但不幸的是,这些药物均宣告临床失败。直到抗体偶联药物(ADC)开始在全球医药圈爆火,靶向FOLR1或FRα疗法在ADC赛道意外出圈,其中以ImmunoGen公司的ADC药物ELAHERE®(mirvetuximab soravtansine-gynx)进展最快,该药已于2022年11月获得了FDA加速批准用于曾接受过 1 至 3 种疗法的FRα+铂耐药上皮性卵巢癌、输卵管癌或原发性腹膜癌患者的治疗。随着FRα在ADC中成药性的证实,目前也有药企针对靶向FRα进行其他赛道的布局,比如双特异性抗体和CAR-T。那FRα究竟是什么?在肿瘤的发展中扮演什么角色?目前靶向FRα的生物疗法竞争格局又是如何?
1、FRα结构与分布
FRα与FRβ、FRγ和FRδ一起都属于叶酸受体(FR)家族,分别有FOLR1、FOLR2、FOLR3和FOLR4基因编码。除FRγ外,FR家族其他成员都 是通过糖基磷脂酰肌醇(GPI)锚定于细胞膜的单链糖蛋白,能够结合叶酸并通过内吞作用转运叶酸进入细胞,是叶酸转运蛋白的一种。人类无法合成叶酸,必须从饮食中获取叶酸。细胞外叶酸的摄取主要通过三种类型的叶酸转运蛋白,分别是还原型叶酸载体RFC(由SLC19A1基因编码)、质子耦合叶酸转运蛋白PCFT(由SLC46A1基因编码)和FR。其中,普遍表达的RFC是叶酸转运至全身组织的主要途径,是一种阴离子反向转运蛋白,利用细胞内较高有机磷酸盐的梯度将叶酸转运入细胞,同时将有机磷酸盐转运出细胞;PCFT将叶酸与质子 (H+ )沿着pH梯度从肠腔的较低pH环境到肠细胞内的较高pH环境耦合起来;而FR 是高亲和力、低通量的转运蛋白,可通过选定组织中的内吞作用转移叶酸。
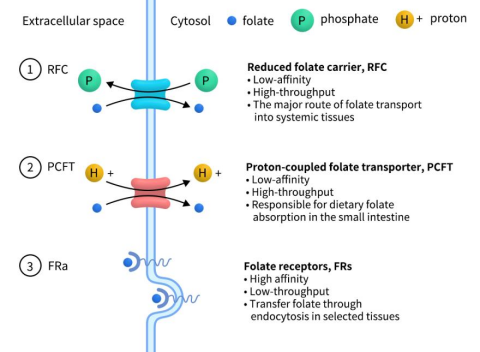
Figure 1. Three types of Folate transporter [1]
如前所述,FRɑ由基因FOLR1编码,该基因位于 11 号染色体,由7个外显子和6个内含子组成。FRɑ蛋白由257aa组成,分子量为30kDa。正常情况下,FRα的组织表达有限,通常局限于极化上皮的管腔(顶端)表面,包括近端肾小管、肺部1型和2型肺细胞、脉络丛、卵巢、输卵管、子宫、子宫颈、附睾、下颌下唾液腺体、支气管腺体和胎盘中的滋养层细胞 [2],这也使该受体不容易接触到叶酸。相比之下,由于FRα 上皮来源的癌症中过度表达,这也使得肿瘤细胞可以直接获取叶酸。
2、FRα在肿瘤中的作用
FRα现已经被证实在正常细胞中几乎不表达,在实体瘤中有广泛高表达,比如间皮瘤(72-100%),三阴性乳腺癌(35-68%),卵巢癌(76-89%),非小细胞肺癌(14-74%);而非恶性组织,只有肺部顶端支气管的上皮细胞,有一定比例的表达。在肿瘤细胞中,FRα不仅可以作为叶酸转运蛋白发挥作用,还可以作为转录因子,在癌细胞增殖、转移的过程中发挥作用。如下图所示,FRα与叶酸结合后,会通过磷酸化启动一系列细胞内信号级联反应,从而激活ERK和STAT3信号途径,从而激活细胞生长的重要调节机制。此外,FRα通过下调细胞间粘附分子E-钙粘蛋白来协助肿瘤侵袭和扩散。
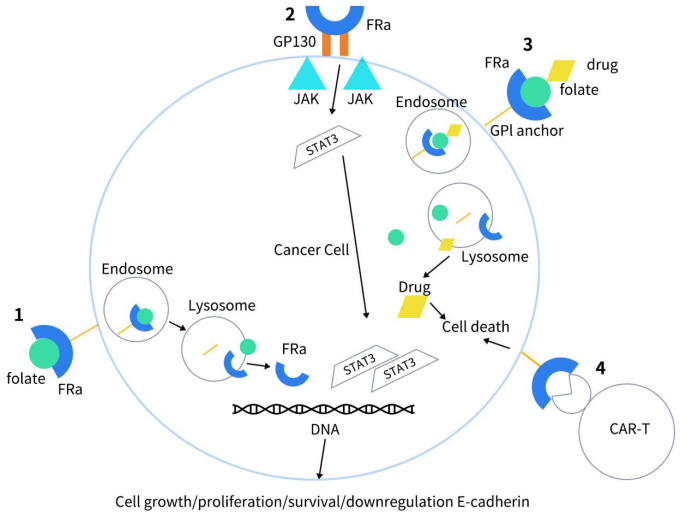
Figure 2. How FRα leads to cell growth [3]
3、FRα靶向疗法研究进展
据不完全统计,目前全球有记录的靶向FRα药物或疗法共计43个,其中处于临床前的有13个,已上市的有1个,当前处于临床阶段的有12个,涉及多种药物类型,包括ADC、单克隆抗体、CAR-T、双特异性抗体和融合蛋白等。
3.1 FRα ADC
目前有记录的靶向FRα的ADC药物共计有21个,处于临床前的有9个,处于临床阶段的有7个,已上市的有1个。是目前临床阶段药物数最多的药物类型。
索米妥昔单抗,又称为mirvetuximab soravtansine-gynx或TAK-853,是由ImmunoGen, Inc.开发的一款靶向FRα的ADC药物。该药物由IgG1亚型抗FRα人源化单抗M9346A、抗微管蛋白剂DM4(一种美登素衍生物)和可裂解连接子三部分组成。是目前唯一一款获批上市的靶向FRα药物,于2022年11月获FDA作为一种单药疗法加速批准,用于治疗先前已接受过1-3种全身治疗方案、FRα+、铂耐药的上皮性卵巢癌、输卵管癌、原发性腹膜癌成人患者。2020年10月,杭州中美华东制药与ImmunoGen签署了总金额为$3.05亿美元战略合作协议。根据协议条款,杭州中美华东制药获得该药在中国大陆、香港、澳门和台湾地区,独家临床开发和商业化权益。2023年8月,Takeda Pharmaceutical与ImmunoGen共同宣布一项合作许可协议。根据合作与许可协议的条款,ImmunoGen将获得一次性$3400万美金的预付款,而Takeda将获得该药在日本独家临床开发和商业化权益。同年11月,AbbVie以$101亿美金的价格首购了ImmunoGen及其肿瘤疗法mirvetuximab soravtansine-gynx。
Luveltamab Tazevibulin,又称为STRO 002,是由Sutro Biopharma开发的一种新型的FOLR1/FRα靶向ADC。该药由IgG1亚型抗FRα单抗、SC209(一种具有抗微管活性的半阿斯特林衍生物)和可裂解连接子三部分组成。Sutro采取XpressCF技术,在合成抗体时定点嵌入非天然氨基酸,从而实现毒素部分的定点偶联,提升ADC药物的均一性,其DAR值为4。目前最高研发状态为临床II/III期(NCT05870748),该项临床研究旨在对比luveltamab tazevibulin和IC化疗对FOLR1表达的卵巢癌(包括输卵管癌或原发性腹膜癌)的疗效和安全性,研究于2023年7月开始,暂时还未有数据公布。2023 ASCO上公布的I期剂量扩展研究(NCT03748186)结果显示:STRO 002针对Frα阳性的晚期卵巢癌患者的ORR达到37.5%。2021年12月,天士力与Sutro Biopharma达成总金额为$3.85亿美元的合作协议。根据协议内容,天力士将获得其靶向FRα的ADC药物,Luveltamab Tazevibulin在中国大陆及港澳台的独家开发和商业化权益。
AZD-5335是AstraZeneca开发的一款靶向叶酸受体α(FRα)的ADC药物,由FRα靶向抗体与AstraZeneca专有的拓扑异构酶1抑制剂(TOP1i)有效载荷(AZ14170132)偶联而成,其DAR值为8。AZD-5335主要作用机制是将AZ14170132送入表达FRα的癌细胞,导致DNA损伤和细胞凋亡。TOP1i有效载荷可以介导旁观者效应,这对于靶向阳性表达不均匀的肿瘤非常重要。目前全球最高研发状态为临床 I/IIa 期(NCT05797168),该项临床试验旨在确定单独使用AZD5335或与抗癌药物联合进行的实验治疗对于晚期肿瘤患者是否安全、可耐受且具有抗癌活性,实验从2023年6月开始,暂时没有数据公布。不过早在2023年AACR上,AstraZeneca公布了AZD5335临床前数据。数据显示,相同或更高剂量下,在FRα低-中表达的两种卵巢癌患者的异种移植模型(PDX)中,AZD5335比基于微管抑制剂(MTI)有效载荷的靶向FRα ADC具有更优秀的临床前活性。
Farletuzumab Ecteribulin,又称为MORAb-202,是卫材研发的一款靶向FRα的ADC药物,由FRα单抗farletuzumab、微管蛋白抑制剂艾日布林和可裂解连接子三部分组成,DAR值为4,具备旁观者效应。2021年6月,BMS与卫材就开发和销售MORAb-202达成总金额为$31亿美元的合作协议,BMS获得MORAb-202美加区域的销售权。该药目前最高研发状态为临床II期(NCT05613088和NCT05577715)。NCT0561308是一项由BMS负责的II期临床试验,该试验的目的是评估MORAb-202的安全性、耐受性和有效性并将其与选择化疗的患有铂耐药卵巢癌、原发性腹膜癌或输卵管癌的女性患者进行比较。NCT05577715是一项由BMS负责的旨在表征MORAb-202的安全性和耐受性,并评估先前接受过治疗的转移性非小细胞肺癌腺癌(NSCLC AC)患者的客观缓解率。
除了以上几款重点介绍的FRα ADC外,目前处于临床阶段的ADC药物还有同宜医药的CBP-1008、普方生物的Rinatabart Sesutecan(又称为Rina-S或PRO1184)、Multitude Therapeutics的AMT-151和百奥泰的BAT8006。此外,还有一波FRα ADC还处于临床前阶段,涉及到的药企有Iksuda Therapeutics(IKS-01和IKS012)、sycivia(antiFRG ADC)、Zymieworks(ZW191)及Mablink Bioscience(MBK103)等。值得注意的是,2023年10月,Mablink Bioscience宣布与礼来达成收购协议,从而获得其独有的psarlink技术平台。
| 药物名称 | 原研机构 | 最高研发状态 |
| 索米妥昔单抗 | ImmunoGen, Inc. | 批准上市 |
| Luveltamab Tazevibulin | Sutro Biopharma, Inc. | 临床II/III期 |
| AZD-5335 | AstraZeneca PLC | 临床II期 |
| Farletuzumab Ecteribulin | 卫材株式会社&BMS | 临床II期 |
| CBP-1008 | 同宜医药 | 临床II期 |
| Rinatabart Sesutecan | 普方生物制药(苏州)有限公司 | 临床I/II期 |
| AMT-151 | Multitude Therapeutics, Inc. | 临床I期 |
| BAT8006 | 百奥泰生物制药股份有限公司 | 临床I期 |
3.2 其他临床阶段的FRα生物药
如前所述,目前处于临床阶段靶向FRα的生物药类型除了ADC,还有单抗、CAR-T、疫苗。其中临床进展最快的是两款疫苗产品,单抗和CAR-T疗法均处于临床I期。此外,还有多款双特异性抗体处于临床前阶段,比如Affmed;Roivant Sciences的AFM32(CD16a/FRa)、Phanes Therapeutics的PT790(FRa/CD3)和PT796(FRa/CD47)两款双抗及TeneoBio开发的TNB-928b等。
| 药物名称 | 药物类型 | 原研机构 | 最高研发状态 |
| ITIL-306 | 肿瘤浸润淋巴细胞 | Instil Bio, Inc. | 临床I期 |
| MOv18 IgE(King’s College London) | 单抗 | 伦敦国王学院 | 临床I期 |
| UB-TT170 | CAR-T | Umoja Biopharma, Inc. | 临床I期 |
| Folate receptor alpha vaccine | 树突状细胞疫苗 | Mayo Clinic | 临床II期 |
| GALE-302 | 治疗性疫苗 | Galena Biopharma | 临床II期 |
4、缔码FRα相关产品与服务,助力FRα靶向疗法开发
缔码生物科技有限公司是一家专注于可成药靶点临床前研发产品和服务的生物技术公司。缔码现可提供FRα靶点全系列产品与服务。产品包括活性蛋白、参照抗体和WB&FC验证单克隆抗体;服务涵盖多种属蛋白抗体定制服务、抗体人源化和亲和力成熟服务。此外,为加速FRα生物疗法的开发,缔码还制备了FRα靶点单B细胞种子库,最快28天可获得先导抗体分子;同时,我们目前已筛选出有52个CDH17先导分子,其中有48个验证了人猴蛋白交叉反应,客户第二天可以拿到分子进行功能评估验证;针对部分分子,我们也正在进行ADC内吞活性及杀伤验证,具体数据欢迎垂询。
- FRα/FOLR1蛋白&抗体
| 产品类型 | 货号 | 产品名称 |
| 重组蛋白 | PME100249 | Human FOLR1 Protein, His Tag |
| PME-C100040 | Cynomolgus FOLR1 Protein, His Tag | |
| PME-M100114 | Mouse FOLR1 Protein, His Tag | |
| WB&FC验证抗体 | DMC100585 | Anti-FOLR1 antibody(18A3), IgG1 Chimeric mAb |
| DMC100391 | Anti-FOLR1 antibody(DMC391); IgG1 Chimeric mAb | |
| 参照抗体 | BME100178 | Anti-FOLR1(mirvetuximab biosimilar) mAb |
| BME100163 | Anti-FOLR1(farletuzumab biosimilar) mAb | |
| 生物素标记抗体 | BME100178B | Biotinylated Anti-FOLR1(mirvetuximab biosimilar) mAb |
| BME100163B | Biotinylated Anti-FOLR1(farletuzumab biosimilar) mAb | |
| DMC100585B | Biotinylated Anti-FOLR1 antibody(18A3), IgG1 Chimeric mAb | |
| DMC100391B | Biotinylated Anti-FOLR1 antibody(DMC391); IgG1 Chimeric mAb |
- FRα/FOLR1先导分子研究进度

参考文献:
[1]Mai J, Wu L, Yang L, Sun T, Liu X, Yin R, Jiang Y, Li J, Li Q. Therapeutic strategies targeting folate receptor α for ovarian cancer.
[2]lnakat H, Ratnam M. Distribution, functionality and gene regulation of folate receptor isoforms: implications in targeted therapy. Adv Drug Deliv Rev. 2004 Apr 29;56(8):1067-84.
[3]Gonzalez, T.; Muminovic, M.; Nano, O.; Vulfovich, M. Folate Receptor Alpha—A Novel Approach to Cancer Therapy. Int. J. Mol. Sci. 2024, 25, 1046.
