2024年3月,一篇题为“Raludotatug Deruxtecan, a CDH6–Targeting Antibody–Drug Conjugate with a DNA Topoisomerase I Inhibitor DXd, Is Efficacious in Human Ovarian and Kidney Cancer Models”的临床前研究发表在《Mol Cancer Ther》上。该研究表明,Raludotatug Deruxtecan,一款有第一三共开发的CDH6 ADC药物对人类卵巢癌和肾癌模型有效。此前,在2023 ESMO大会上也公布了Raludotatug Deruxtecan单药治疗既往经治卵巢癌患者的首次人体I期研究(NCT04707248)亚组分析结果,结果显示确认客观缓解率46%,疾病控制率可达98%。既然CDH6如此优秀,那我们就来聊聊背景和当前靶向药布局吧。
1、CDH6与经典钙粘蛋白
钙粘附蛋白6(CDH6),又称为胎儿肾钙粘蛋白或K-钙黏蛋白,是由790个氨基酸构成的单次跨膜蛋白,属于II型经典钙黏蛋白,为钙粘蛋白超家族成员之一。钙粘蛋白超家族由四个主要亚家族组成:经典钙粘蛋白、桥粒钙粘蛋白、原钙粘蛋白和非典型钙粘蛋白[1]。如下图所示,经典钙黏蛋白由三部分组成,一个胞外域、一个跨膜域和一个胞内域,其中,胞外域含有五个钙粘蛋白结构域(EC1-EC5)。胞外结构域(主要是N端结构域EC1)在两个钙粘蛋白分子之间的同源识别中起关键作用。
经典钙粘蛋白会根据第一个EC结构域中是否含有组氨酸-丙氨酸-缬氨酸(HAV)基序进一步细分为 I型和II型。I型钙粘蛋白分子仅包含五个成员:上皮钙黏蛋白(E-Cadherin或CDH1)、神经钙黏蛋白(N-Cadherin或CDH2)、胎盘钙黏蛋白(P-Cadherin或CDH3)、肌微管钙黏蛋白(M-Cadherin或CDH15)和视网膜钙黏蛋白(R-Cadherin或CDH4);CDH5-12、CDH18-20、CDH22和CDH24为II型钙粘蛋白分子。除了HAV基序的差异,I型和II型钙粘蛋白在一些氨基酸残基上也存在差异。
钙黏蛋白分子的构象仅在Ca2+存在下稳定,Ca2+与多肽链的细胞外部分的结合是钙粘蛋白介导的细胞间粘附的先决条件。由短的高度保守氨基酸序列组成的钙结合位点位于相邻的细胞外重复序列之间[2]。经典钙粘蛋白的胞质域可与p120-catenin和β-catenin结合,而钙黏连蛋白家族的其他成员(包括原钙粘蛋白)不结合连环蛋白。

Figure 1. The structure of classical Cadherins [3]
在人类中,钙粘蛋白-6是一种由CDH6(又称为CAD6或KCAD)基因编码的蛋白质,编码该蛋白的基因位于五号染色体上。与其他II型经典钙黏蛋白不一样的是,CDH6 在EC1结构域包含RGD基序,在EC5包含HAV基序,用于稳定和聚集相邻单体。与其他经典钙黏蛋白一样,CDH6的胞质尾可与p120-catenin和β-catenin结合来调节肌动蛋白细胞骨架。由于β-catenin在Wnt 信号通路中的核心作用,β-catenin信号转导与 CDH6 介导的细胞间粘附之间存在联系[4]。
CDH6参与胚胎肾脏的形态发生和发育,并驱动肾脏形态发生所必需的间充质-上皮分化,但在成人肾脏中,CDH6的表达非常弱。在成年人的正常组织中,CDH6的表达局限于肾脏的肾小管、胆管上皮细胞等。此外,CDH6也在血小板中表达,在血小板聚集和血栓形成中起功能性作用。该功能由RGD 基序与αIIbβ3整合素结合介导,后者发生构象变化并与纤维蛋白原结合,从而交联血小板[5]。
2、CDH6与肿瘤
据报道,CDH6在甲状腺癌、胃癌、胰腺癌和卵巢癌中高表达,其中,肾癌是最早发现CDH6高表达的癌症。

Figure 2. The expression of CDH6 in various tumors (*Data derived from The Human Protein ATLAS)
关于CDH6在癌症中的作用机制尚不完全清楚,但Rubén A. Bartolomé等人研究表明,CDH6和相关整合素在卵巢癌和肾癌进展中发挥的关键作用。如下图所示:在αIIbβ3高表达的细胞中,CDH6 就会优先结合αIIbβ3,从而诱导α2β1整合素的激活。整合素的激活会促进细胞粘附、侵袭和增殖,从而导致癌细胞的转移性播散;在αIIbβ3低表达的细胞中,CDH6和CDH17与α2β1 整合素结合,这种钙粘蛋白/整合素相互作用通过激活SRC、FAK、AKT和ERK通路促进细胞粘附、迁移、侵袭和增殖。

Figure 3. CDH6 and αIIb/α2 integrins are required for lung homing in ovarian and renal cancer [6]
3、CDH6靶向疗法当前研究进展
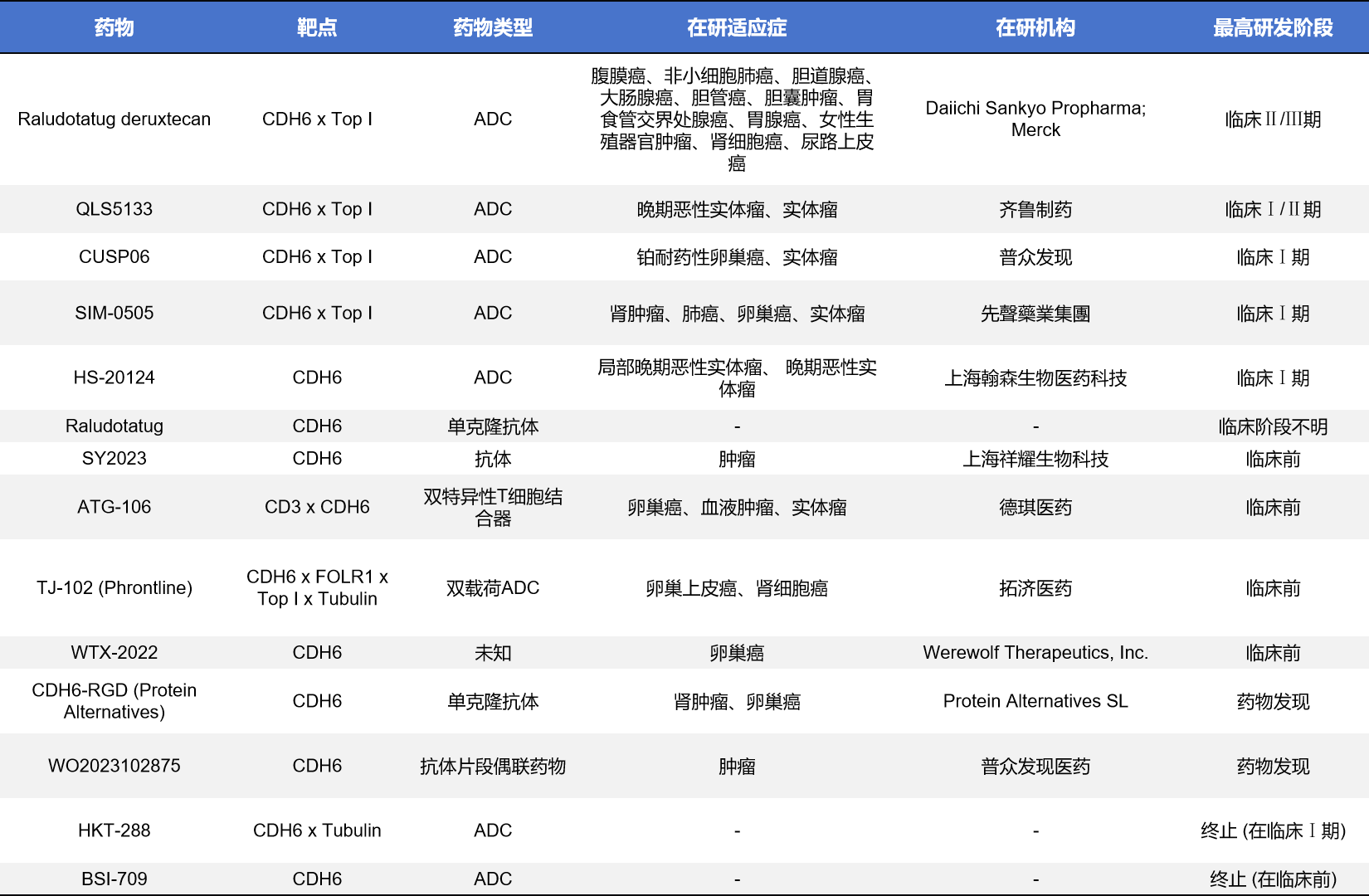
如前所述,CDH6是钙粘蛋白家族的II类经典成员,参与细胞-细胞黏附和组织发育。在正常成人组织中表达很低,但在多种实体肿瘤(尤其是卵巢癌、肾细胞癌)中高表达,与肿瘤侵袭、转移和较差预后显著相关,因此成为一个有前景的肿瘤治疗靶点。不完全统计,目前全球靶向CDH6的在研疗法有14款,5款处于临床阶段,4款处于临床前,2款处于药物发现,2款已终止。值得注意的是,进入临床的全是抗体偶联药物(ADC)。
- Raludotatug deruxtecan
Raludotatug deruxtecan,代号为DS-6000或R-DXd,是第一三共开发的一款靶向CDH6的ADC药物。R-DXd由人源化的CDH6 IgG1单抗、可剪切linker及DXd组成,采用的是第一三共标志性的“GGFG四肽linker和Dxd”的组合,DAR值为8。2024年2月,针对适应症卵巢癌被欧盟授予孤儿药称号。早期的I期临床(NCT04707248)研究显示,R-DXd单药对晚期卵巢癌患者治疗效果积极,总体缓解率(ORR)为46%,疾病控制率(DCR)为98%,中位缓解持续时间(mDoR)为11.2个月。目前,第一三共正在与默克联合推进针对铂耐药性卵巢癌患者的一项II/III期(NCT06161025)临床研究。
- QLS5133
QLS5133是由齐鲁制药自主研发的一款靶向CDH6的ADC,用于治疗CDH6高表达的晚期实体瘤。该药物采用人源化抗CDH6单克隆抗体,通过可裂解连接子偶联拓扑异构酶I抑制剂载荷(QLS6916),具备较高的DAR值(约8),在介导肿瘤细胞内吞后释放细胞毒性药物,从而实现精准杀伤,并可能产生一定旁观者效应。2025年,QLS5133获得中国国家药监局(CDE)批准开展临床试验,目前处于I/II期临床研究阶段,旨在评估其在晚期实体瘤患者中的安全性、耐受性、药代动力学特征及初步抗肿瘤疗效,适应症探索方向包括卵巢癌、输卵管癌、原发性腹膜癌及肾细胞癌等CDH6高表达肿瘤。目前,QLS5133临床试验已正式启动并进入患者招募阶段,相关临床前研究数据显示其在多种CDH6阳性肿瘤模型中表现出显著抑瘤活性和相对可控的安全性,为其后续临床推进提供了重要依据。
- CUSP06
CUSP06,又称为AMT-707,是普众发现(Multitude Therapeutics, Inc.)开发的一款CDH6 ADC药物,由与CDH6具有高结合亲和力的专有抗体、蛋白酶可切割的连接子,以及依沙替康有效载荷(一种TOP1抑制剂)三部分组成,DAR值为8,目前的最高研发状态为临床I期(NCT06234423)),针对的适应症为晚期恶性实体瘤和铂耐药性卵巢癌。2022年6月,普众发现与昂阔医药(OnCusp Therapeutics)就AMT-707(现称为CUSP06)的开发和商业化达成许可协议。根据协议,昂阔医药将获得在大中华区以外的全球范围内独家开发和商业化AMT-707的权利。而普众发现将获得预付款、开发、注册和销售里程碑付款以及分级特许权使用费。
临床前研究数据显示,CUSP06与基于DXd的CDH6 ADC具有更强的“旁观者效应”。CUSP06 选择性地与细胞表面CDH6结合,并有效地内化到 CDH6 阳性卵巢癌细胞和肾癌细胞中。CUSP06在体外对几种CDH6阳性癌细胞系表现出强大的抗增殖活性。此外,经CUSP06治疗的两种CDH6低表达和高表达患者来源的异种移植(PDX)模型中也观察到肿瘤消退[7]。
- SIM-0505
SIM-0505是一款由先声再明(Simcere Zaiming)研发的CDH6 ADC,采用差异化抗体表位并偶联拓扑异构酶I抑制剂载荷,旨在精准靶向CDH6高表达的实体瘤细胞,如卵巢癌、肾细胞癌等。临床前研究显示,该分子在多种肿瘤模型中具有较强的抗肿瘤活性和相对可控的安全性。SIM-0505目前处于I期临床阶段,已在中国启动剂量递增试验,并于2025年推进至美国开展I期临床研究,重点评估其安全性、耐受性、药代动力学及初步疗效,标志着项目进入全球同步开发阶段。此外,2025年,SIM-0505还完成一项重要国际授权合作:先声再明与NextCure达成战略协议,授予其除大中华区以外的全球开发和商业化权益,交易总潜在金额最高约7.45亿美元,包括里程碑付款及销售分成。该合作显著提升了SIM-0505的全球化开发价值与市场关注度。
- HS-20124
HS-20124是由翰森制药(Hansoh Pharmaceutical)自主研发的一款CDH6 ADC候选药物,采用DAR=8设计结合拓扑异构酶抑制剂载荷,旨在精准识别并杀伤CDH6高表达的实体瘤细胞。HS-20124在临床前研究中表现出对CDH6阳性肿瘤细胞的抑制效应,为进入人体试验奠定基础。目前,HS-20124正处于临床I期研究阶段。登记为NCT06763159的开放标签、多中心I期Ia/1b试验自2024年10月启动,涵盖剂量递增和剂量扩展队列,旨在评估其安全性、耐受性、药代动力学特征以及初步抗肿瘤活性,预计试验将于2027年底完成。该研究计划纳入约450名晚期实体瘤患者,并在扩展队列中探讨特定肿瘤类型的疗效表现。
- HKT-288
HKT-288,又称为NOV-13,是Novartis Pharma AG开发的一款CDH6 ADC药物,包含对CDH6 具有选择性的全人源抗体、可裂解连接子SPDB和DM4组成。目前该药已止步于临床I期,这项首次人体研究(NCT02947152)中,0.75 mg/kg剂量治疗组的患者报告了三例疑似相关的神经系统2级不良反应:1名患者癫痫发作,另一名患者失语和脑病。进一步的研究无法确定神经系统不良反应的潜在机制,因此该研究提前终止。此外,处于临床前阶段的还有德琪(浙江)医药科技有限公司(Antengene Corporation Co., Ltd.)开发的双特异性抗体ATG-106(CD3 x CDH6)和博奥信生物技术(南京)有限公司(Biosion, Inc.)开发的CDH6 ADC药物BSI-709,其中BSI-709项目已终止。而Protein Alternatives SL开发的单克隆抗体CDH6-RGD目前还处于药物发现阶段。
4、缔码CDH6相关产品助力CDH6生物药开发
缔码生物科技有限公司是一家专注于可成药靶点临床前研发产品和服务的生物技术公司。缔码现可提供CDH6靶点全系列产品与服务。产品包括活性蛋白、参照抗体和流式验证单克隆抗体;服务涵盖多种属蛋白抗体定制服务、抗体人源化和亲和力成熟服务。此外,为加速CDH6生物疗法的开发,缔码还制备了CDH6靶点单B细胞种子库,最快28天可获得先导抗体分子;同时,我们目前已筛选出有26个CDH6先导分子,均为人猴交叉分子,其中25个跟鼠也有交叉反应,客户第二天可以拿到分子进行功能评估验证;针对部分分子,我们也正在进行ADC内吞活性及杀伤验证,具体数据欢迎垂询。
- CDH6蛋白&抗体&过表达细胞株&移植瘤切片
| 产品类型 | 产品货号 | 产品名称 |
| 重组蛋白 | PME101111 | Human CDH6 Protein, His Tag |
| PME-C100044 | Cynomolgus CDH6 Protein, His Tag | |
| PME-M100112 | Mouse CDH6 Protein, His Tag | |
| 流式抗体 | DMC100675 | Anti-CDH6 antibody(DMC675); IgG1 Chimeric mAb |
| 参照抗体 | BME100232 | Anti-CDH6(raludotatug biosimilar) mAb |
| BME100234 | Anti-CDH6(AMT-707 biosimilar) mAb | |
| 生物素标记抗体 | BME100232B | Biotinylated Anti-CDH6(raludotatug biosimilar) mAb |
| DMC100675B | Biotinylated Anti-CDH6 antibody(DMC675); IgG1 Chimeric mAb | |
| 过表达细胞株 | CEL100055 | Hu_CDH6 CHO-S Cell Line |
| 移植瘤切片 | SLI100004 | Balb/C nu HuH7 DiSliceX™ SlideSet |
- CDH6先导分子研究进度

参考文献:
[1]Brasch, J., Harrison, O. J., Honig, B., & Shapiro, L. Thinking outside the cell: how cadherins drive adhesion. Trends in cell biology, 2012, 22(6), 299–310.
[2]Ivanov DB, Philippova MP, Tkachuk VA. Structure and functions of classical cadherins. Biochemistry (Mosc). 2001, Oct;66(10):1174-86.
[3]Basu, R., Taylor, M. R., & Williams, M. E. (2015). The classic cadherins in synaptic specificity. Cell adhesion & migration, 9(3), 193–201.
[4]Stewart DB, Barth AI, Nelson WJ. Differential regulation of endogenous cadherin expression in Madin-Darby canine kidney cells by cell-cell adhesion and activation of beta -catenin signaling. J Biol Chem. 2000 Jul 7;275(27):20707-16.
[5]Casal, J. I., & Bartolomé, R. A. Beyond N-Cadherin, Relevance of Cadherins 5, 6 and 17 in Cancer Progression and Metastasis. International journal of molecular sciences,2019,20(13), 3373.
[6]Bartolomé, R. A., Robles, J., Martin-Regalado, Á., et al. CDH6-activated αIIbβ3 crosstalks with α2β1 to trigger cellular adhesion and invasion in metastatic ovarian and renal cancers. Molecular oncology, 2021, 15(7), 1849–1865.
[7]Wei Lu, Jing Shi, Shu-Hui Liu, Nicole Covino, Xun Meng, Eric D. Slosberg. CUSP06/AMT-707, a new CDH6-targeting antibody-drug conjugate, demonstrates potent antitumor activity in preclinical models [abstract]. In: Proceedings of the American Association for Cancer Research Annual Meeting 2023; Part 1 (Regular and Invited Abstracts); 2023 Apr 14-19; Orlando, FL. Philadelphia (PA): AACR; Cancer Res 2023;83(7_Suppl):Abstract nr 6320.



