2024年9月25日,天境生物宣布,已与赛诺菲(Sanofi)就CD73抗体尤莱利单抗(uliledlimab)在大中华区的开发、生产和商业化达成潜在总价近2.13亿欧元(约合17亿人民币)的战略合作。uliledlimab是天境生物自主研发的创新CD73单抗,可通过调节肿瘤微环境增强机体对癌细胞的免疫应答。今天,我们就具体聊聊CD73生物背景及其靶向药的研究进展。
1、CD73结构
CD73,又称为外-5′-核苷酸酶或5’-核苷酸酶(5’-NT),是一种由NT5E基因编码的糖基磷脂酰肌醇(GPI)锚定细胞表面蛋白。人类NT5E基因位于染色体6q14.3上,编码的CD73蛋白包含574个氨基酸。如Figure 1所示,CD73是一种二聚化的外5-核苷酸酶 (5’-NT),在质膜外侧表达.。每个亚基由三个结构域组成,其中N端包含两个金属离子结合位点,C端有一个底物结合位点,α-螺旋形成一个灵活的连接区,CD73通过GPI锚连接到细胞膜上 [1]。
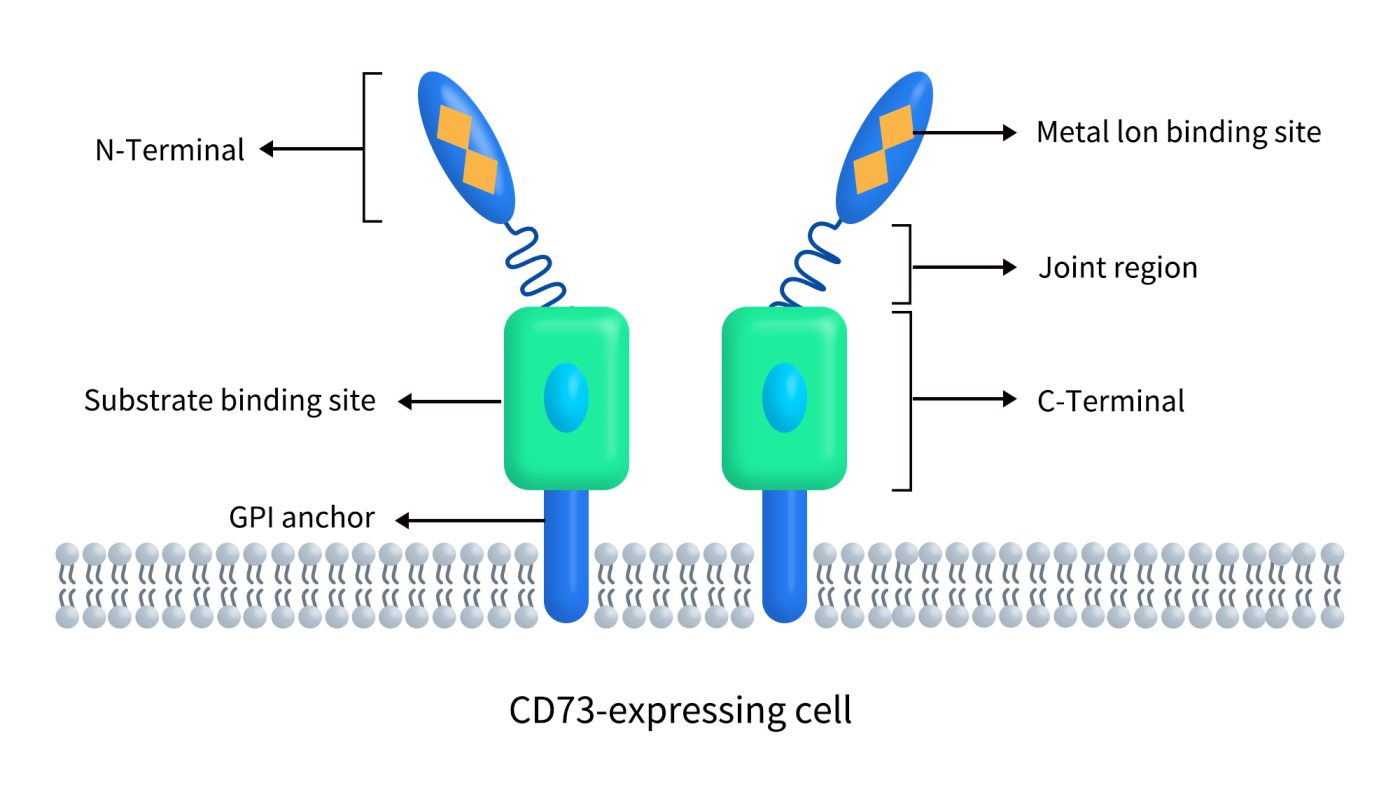
Figure 1. The structure of CD74 [1]
2、CD73的分布与功能
CD73 存在于多种细胞类型的表面,包括内皮细胞、淋巴细胞亚型、基质细胞和某些类型的肿瘤细胞。CD73对5′-腺苷-磷酸(5′-AMP)生成细胞外腺苷至关重要,是嘌呤信号通路的重要组成部分,该过程通过CD39的协同作用进行。CD39(也称为ENTPD1)可催化ATP和ADP的磷酸水解为腺苷一磷酸(AMP)。细胞外ATP主要由几种统称为外核苷酸酶的酶快速代谢,包括外核苷三磷酸二磷酸水解酶(ENTPD)和外核苷酸焦磷酸酶/磷酸二酯酶 (ENPP) 蛋白家族的成员。除了CD39,ENPP1也可催化ATP生成AMP。然后,CD73会将AMP进一步水解为腺苷。腺苷可激活四种G蛋白偶联腺苷受体(AR),包括A1R(ADORA1)、A2AR(ADORA2A)、A3R(ADORA3)和A2BR(ADORA2B)。这些受体对腺苷具有不同的亲和力,亲和力由大到小依次为:A1R、A2AR、A3R 和A2BR,前三种受体的亲和力均远大于A2BR。可激活多种信号通路来控制氧气供需、炎症和其他生理活动,具体是激活哪种信号通路这取决于细胞类型和受体表达模式[2]。此外,腺苷还可以通过平衡核苷转运蛋白(ENT)被吸收,并在细胞内重新磷酸化为AMP [3]。作为细胞外腺苷的主要酶源,CD73是许多组织中细胞稳态、应激反应、损伤和疾病机制的关键调节器[4]。
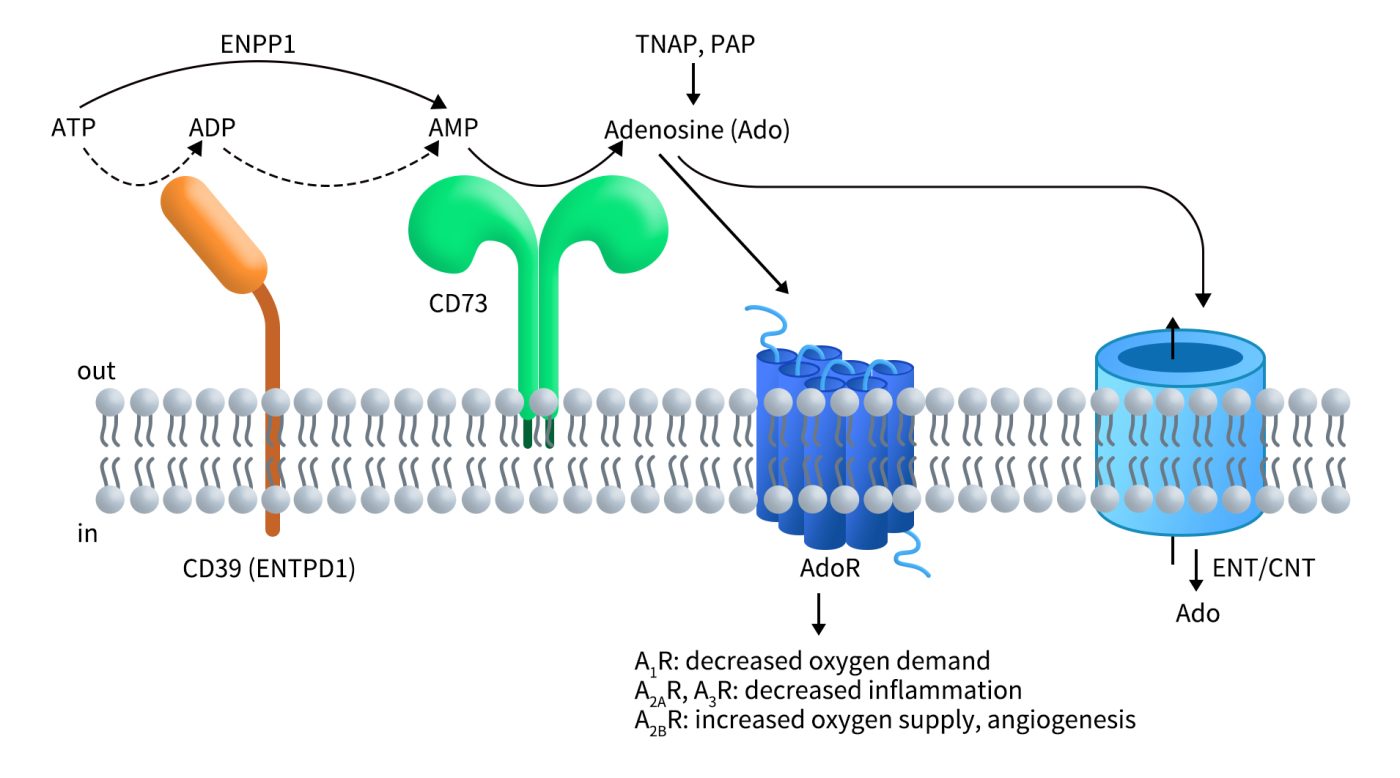
Figure 2. CD73 is an essential component of purinergic signaling [5]
3、CD73与肿瘤
近年来,嘌呤信号通路已成为癌症进展中的重要参与者,其中细胞外ATP、ADP和腺苷作为主要信号分子[6]。免疫抑制代谢物-腺苷是肿瘤微环境(TME)的一个组成部分。作为催化腺苷生产的主要酶,CD73主要通过产生腺苷,在抑制足够的抗肿瘤免疫反应方面至关重要,但也促进癌细胞增殖、肿瘤生长、血管生成和转移。如Figure 3所示,TME中受损或死亡细胞释放的ATP是免疫细胞的危险信号,主要通过P2X和P2Y受体发出信号来促进抗肿瘤免疫反应,这些受体在不同细胞类型中存在差异表达。ATP在CD39和CD73 的协同作用下降解为腺苷。腺苷通过A2A和A2B受体信号传导抑制免疫细胞,或通过直接增强肿瘤细胞增殖、血管生成、上皮-间质转化 (EMT) 和转移来促进肿瘤生长。

Figure 3. ATP and adenosine signalling in the tumour microenvironment (TME) [7]
CD73 在多种癌细胞系和患者活检中均有过表达,但不同的癌症类型表达程度不一样。CD73 在胶质母细胞瘤、甲状腺癌、肉瘤、胰腺癌、胃腺癌、结直肠癌、肾细胞癌、食道癌、胸腺瘤、直肠腺癌、肺腺癌、非小细胞肺癌和急性髓细胞白血病中表达较高。在泌尿生殖系统癌症以及黑色素瘤、乳腺癌和胆管癌中观察到CD73表达较低 [7]。
4、CD73靶向药物的临床研究进展
越来越多的研究表明,CD73 是癌细胞增殖、迁移和侵袭(体外),肿瘤血管生成和肿瘤免疫逃逸(体内)的关键调控分子。基于这些作用,CD73 已成为一个有吸引力的治疗靶点。不完全统计,全球靶向CD73的药物共计89款,其中临床前药物有34款,临床阶段药物有26款,临床申请批准阶段的有5款。尽管暂无靶向CD73的药物上市,但药物类型多样化,涉及单克隆抗体、抗体偶联药物(ADC)、双特异性抗体、小分子化药及融合蛋白等,这也证明了CD73靶点的潜力之大。其中在研药物数量最多的药物类型是单克隆抗体,这里重点展示了处于临床及临床申请阶段的靶向CD73药物研究进展。
4.1 CD73单克隆抗体
目前全球处于临床阶段的靶向CD73的单克隆抗体药有18款,其中包含一款未注明抗体类型的抗体药S-095024。在这18款临床阶段药物中,有9款处于临床1期,2款处于临床2期,仅有1款处于临床3期。布局企业国外以阿斯利康、Halozyme Therapeutics和BMS为代表,国内以天境生物、信达生物及和铂医药为代表。

Oleclumab是由阿斯利康开发的一款全人源化IgG1λ CD73单克隆抗体(mAb),是全球临床进展最快的CD73 mAb药物。Oleclumab的重链恒定区发生三重突变,导致IgG效应功能降低,从而诱导CD73内化以抑制其活性。在小鼠结肠癌模型中, oleclumab减轻了AMP诱导的T细胞增殖抑制,显著抑制了肿瘤生长,增加了肿瘤浸润中CD8+和髓样细胞的百分比,并增强了抗原呈递的潜力。目前,Oleclumab正被开发用于治疗多种实体瘤:非小细胞肺癌(NSCLC),胰腺癌等。全球最高研发阶段为临床III期。
Uliledlimab是天境生物自主研发的一款高度差异化的人源化IgG1κ CD73 mAb,是目前全球临床进展第二的CD73 mAb药物。该抗体耐受性良好,无剂量限制性毒性,能够饱和循环和细胞结合CD73,通过调节肿瘤微环境增强机体对癌细胞的免疫应答。在2023 ASCO年会上,天境生物公布了在美国和中国开展的1b/2期临床研究数据。数据显示,Uliledlimab与特瑞普利单抗联用用药在CD73高表达NSCLC患者中安全性良好且疗效显著。当前全球最高研发阶段为临床2/3期。
S-095024是一款未注明抗体类型的CD73抗体药。该药是由Servier Bio-Innovation开发的一种完全人源化、效应功能减弱抗体,可与人类和食蟹猴CD73以亚nM亲和力结合。在2024 ASCO年会上公布的早期临床数据揭示了S095024阻止腺苷介导的肿瘤逃逸的潜力,并支持进一步的临床研究。
4.2 CD73双特异性抗体
靶向CD73的双特异性抗体以中山康方生物的AK131为代表,这也是全球唯一一款进入临床阶段的CD73双特异性抗体。AK131是一款靶向PD-1与CD73的双特异性抗体,由AK105(PD-1单抗)和AK119(CD73单抗)衍生而来。AK119不仅可抑制CD73活性及腺苷产生,还可刺激B细胞活化。AK131则可有效完全抑制CD73的酶学活性,阻断PD-1介导的免疫细胞抑制。康方生物在2022 AACR年会上公布的AK131临床前研究数据表明,AK131显示出强大的体内外活性。AK131除能有效阻断PD-1/PDL-1相互作用,还可有效地促进T细胞和B细胞的活化,诱导CD73的内吞作用。

4.3 靶向CD73的小分子化药
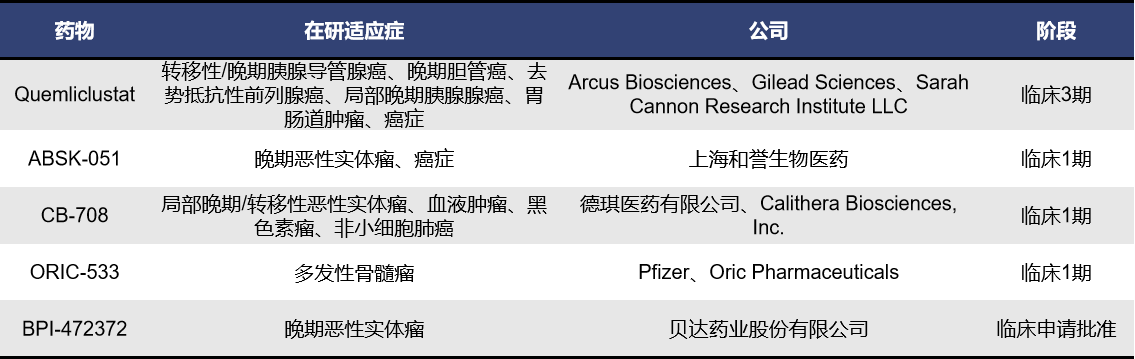
目前进入临床阶段的靶向CD73小分子化药共有5款,其中全球临床进展最快的是Quemliclustat。Quemliclustat是由Arcus Biosciences开发的一款靶向CD73的小分子抑制剂,可通过有效阻断TME中腺苷产生来抑制AMP和细胞外腺苷介导的肿瘤免疫抑制。该药于2024年9月23日启动III期临床(PRISM-1/NCT06608927),成为首个进入III期阶段的小分子CD73抑制剂。NCT06608927旨在评估Quemliclustat联合化疗(白蛋白紫杉醇+吉西他滨)对比安慰剂联合化疗治疗未接受过治疗的转移性胰腺导管腺癌(PDAC)患者的疗效和安全性。
4.4 CD73 ADC
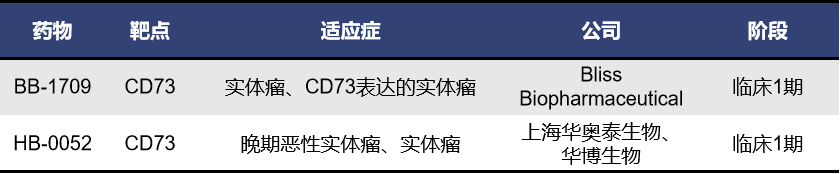
目前进入临床的CD73 ADC药物共两款,百力司康的BB-1709和华奥泰的HB-0052,二者均处于临床1期。有研究表明,与未偶联的CD73裸抗相比,CD73 ADC能够引发促炎巨噬细胞和活化树突状细胞(DC)在肿瘤内大量聚集,同时CD73 ADC还具有保护效应T细胞和刺激DC的功能,在杀伤CD73高表达肿瘤和改善肿瘤免疫应答方面具有双重优势[8]。具体效果还有待于进一步临床验证。
5、缔码CD73相关产品与服务助力CD73生物疗法开发
缔码生物科技有限公司是一家专注于可成药靶点临床前研发产品和服务的生物技术公司。缔码现可提供HER3靶点全系列产品与服务。产品包括活性蛋白、参照抗体和流式验证单克隆抗体;服务包括多种属蛋白抗体定制服务、抗体人源化和亲和力成熟服务。此外,为加速CD73生物疗法的开发,缔码还制备了CD73靶点单B细胞种子库,最快28天可获得先导抗体分子;同时,我们目前已筛选出多个CD73先导分子,客户第二天可以拿到分子进行功能评估验证。
- CD73蛋白&抗体&CDX切片
- 缔码CD73先导分子研究进展

参考文献:
[1] Zandieh, K., Millani, S., Mohammadi, J., et al. Therapeutic Value of CD73 as a Biomarker in Human Cancer. Archives of Advances in Biosciences, 2019, 10(3), 45–54.
[2] Borea PA, Gessi S, Merighi S, et al. Pharmacology of Adenosine Receptors: The State of the Art. Physiol Rev. 2018 Jul 1;98(3):1591-1625.
[3] Pastor-Anglada M, Pérez-Torras S. Who Is Who in Adenosine Transport. Front Pharmacol. 2018 Jun 14;9:627.
[4] Minor M, Alcedo KP, Battaglia RA, et al. Cell type- and tissue-specific functions of ecto-5′-nucleotidase (CD73). Am J Physiol Cell Physiol. 2019 Dec 1;317(6):C1079-C1092.
[5] Alcedo, Karel P. et al. The elegant complexity of mammalian ecto-5’-nucleotidase (CD73). Trends in Cell Biology, 31 (10), 829 – 842.
[6] Burnstock G. and Di Virgilio F., Purinergic signalling and cancer, Purinergic Signalling. 2013, 9, no. 4, 491–324.
[7] Bach, N., Winzer, R., Tolosa, E., et al. The Clinical Significance of CD73 in Cancer. International journal of molecular sciences, 2023, 24(14), 11759.
[8] Jin R, Liu L, Xing Y, et al. Dual Mechanisms of Novel CD73-Targeted Antibody and Antibody-Drug Conjugate in Inhibiting Lung Tumor Growth and Promoting Antitumor Immune-Effector Function. Mol Cancer Ther. 2020 Nov;19(11):2340-2352.



