2020 年末,Genmab和ADC Therapeutics分别宣布终止Enapotamab vedotin和ADCT-601的临床开发,因为两款药在早期试验中未达到预期效果。Enapotamab vedotin和ADCT-601都是靶向AXL的ADC药物。不同的是,Enapotamab vedotin偶联的是微管类抑制剂MMAE, ADCT-601偶联的是PBD二聚体细胞毒素(更多关于ADC毒素>>)。2023年1月,BioAtla公布了BA-3011(CAB-AXL-ADC)最新临床数据,数据未呈现出明显的积极效果。数据一出,BioAtla股价大跌46%。BA-3011是一款基于CAB技术设计来的靶向AXL的ADC药物。据不完全统计,目前靶向AXL的临床药共计有29款,3款ADC,1款CAR-T,1款抗体,24款小分子药物(包含2款已上市的小分子药物)。而AXL-ADC药物接二连三的失利,让靶向AXL的免疫疗法陷入低谷。那AXL靶点的作用机理究竟是什么?当前靶向AXL的免疫疗法布局又是如何?
1、AXL结构与分布
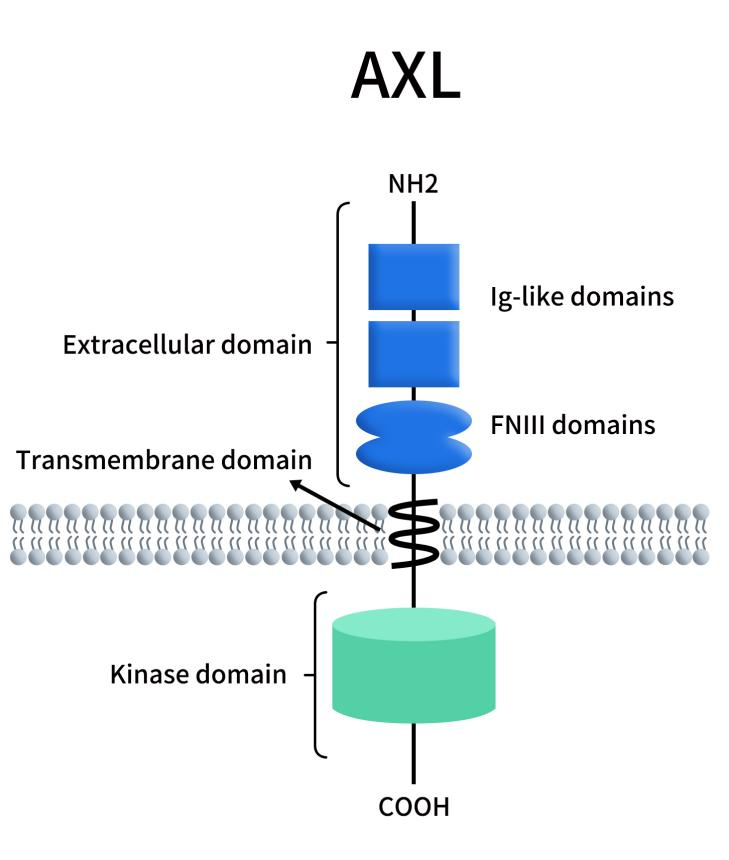
AXL,又名 Ark,Ufo和Tyro-7,是一种受体酪氨酸激酶,最初是Liu E等人1988年在筛选粒细胞白血病(CML)慢性转急性相关的基因时发现的[1]。人类AXL基因位于染色体19q13.2,编码20个外显子。如Figure 1所示,AXL蛋白含有894个氨基酸,分子量为104kDa,分为胞外区、跨膜区和胞内区[2]。胞外区由外显子1-10编码,包括信号肽、两个免疫球蛋白(Ig)结构域和两个纤连蛋白Ⅲ型(FNⅢ)结构域;整个跨膜结构域和一个受蛋白水解切割的短的细胞外区域由外显子11编码;外显子12-20编码细胞内结构域,包括酪氨酸激酶结构域。胞内结构域对于自身磷酸化和活化后的激酶活性至关重要,可参与正常细胞及肿瘤细胞多种信号的传递 [3]。
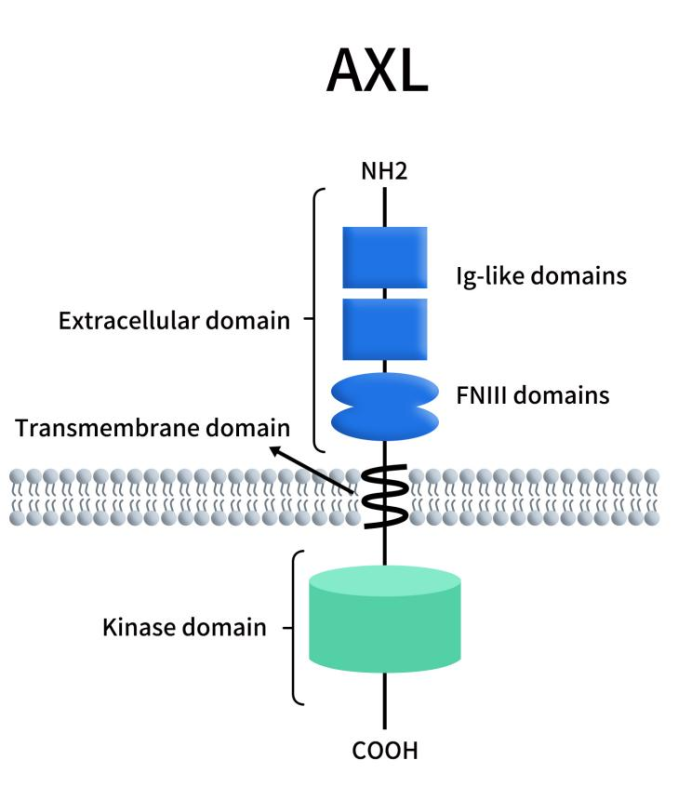
Figure 1. The structure of AXL [4]
正常生理条件下,AXL的表达大多局限于正常细胞中的平滑肌、肺、肾、睾丸和血液 [5]。在对许多癌细胞的研究中发现,AXL在非小细胞肺癌、乳腺癌、卵巢癌等多种癌症中高表达,与肿瘤的发生、发展以及耐药密切相关。
2、AXL信号通路
如前所述,AXL与其他TAM 家族受体一样,为了响应炎症反应等各种生物过程,一般是通过经典的配体结合整合细胞外信号,从而诱导有效的细胞内信号传导。而AXL激活存在两种方式,一种是经典的配体依赖性激活(为主),一种是非Gas6依赖性激活。AXL经典的配体依赖性激活指的是AXL/Gas6信号通路。AXL受体的非Gas6依赖性激活指的是AXL与另外2个TAM受体(Mer和Tyro-3)和其他几种非TAM家族成员蛋白(如:EGFR、HER2等)相互作用来激活。这里重点介绍AXL/Gas6这条主要作用通路。
如下图所示,当AXL的Ig结构域与GAS6结合形成复合物时,该复合物与另一个GAS6-AXL复合物二聚化,形成 2:2 同源二聚化复合物。Axl受体二聚体后,AXL受体胞内域中的酪氨酸残基会发生反式自磷酸化。AXL胞内激酶结构域中共有6个磷酸化位点,其中 3个C端的磷酸化位点(Y698、Y702和Y703)在TAM保守,另外3个N端(Y779,Y821和Y866)则会发生自磷酸化并参与对接和激活。AXL胞内域中酪氨酸残基磷酸化是招募胞内接头分子和效应蛋白并最终激活下游信号通路所必需的。AXL激活后会启动许多下游通路的信号传导,例如 PI3K/AKT、MAPK/ERK和 PKC。这些信号传导的激活在细胞活动中起到多种不同作用,比如细胞增殖和存活、迁移和侵袭、上皮间质转化 (EMT)、血管生成、治疗抵抗、免疫抑制和干细胞维持激活功能[6]。
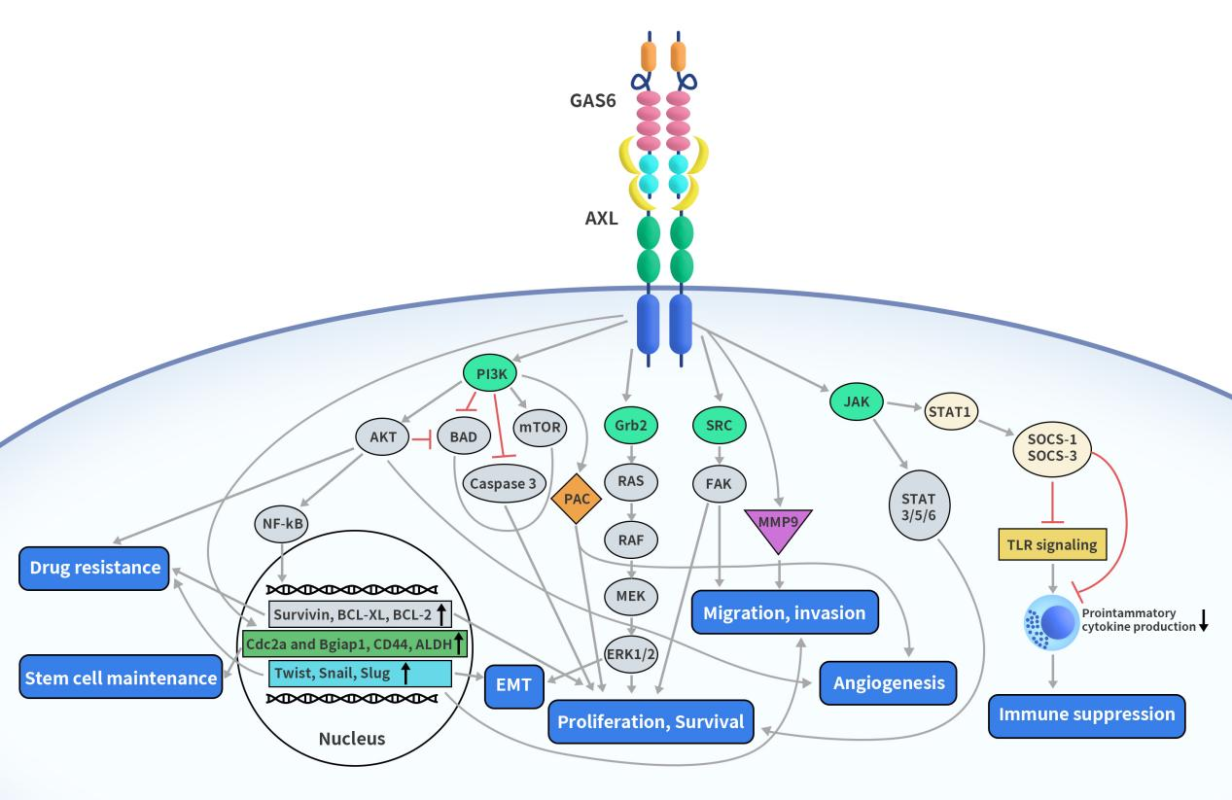
Figure 2 AXL signaling pathway[3]
3、AXL靶向药研究进展
据Clinical trail数据展示,目前靶向AXL的临床药还是以小分子化合物为主,以免疫疗法为基础的药只有5款,3款ADC,1款CAR-T,1款抗体。
3.1 AXL-ADC
Enapotamab vedotin,亦称为AXL-107-MMAE,是一种靶向Axl的抗体药物偶联物 (ADC),DAR值为4。Enapotamab vedotin 由 Genmab 全资拥有,通过蛋白酶可切割的缬氨酸-瓜氨酸连接子将AXL特异性IgG1与甲基澳瑞他汀E(MMAE)偶联起来,该连接技术连已获得Seagen Inc.的许可。目前临床上针对的适应症是实体瘤,包括卵巢癌、非小细胞肺癌(NSCLC)、子宫内膜癌、宫颈癌和甲状腺癌。当前最高研发阶段为临床二期。临床前研究表明,Enapotamab vedotin 在NSCLC模型中表现出显著的抗肿瘤活性[7]。但遗憾的是,Enapotamab vedotin疗效与剂量不符合Genmab继续开发的概念验证标准。在2020年11月25日,Genmab宣布终止Enapotamab vedotin的临床开发。
Mipasetamab uzoptirine,亦称为ADCT-601,是一种AXL靶向抗体-药物偶联物,由人源化抗 AXL IgG1抗体、Val-Ala可裂解连接子和有效的吡咯并苯二氮卓 (PBD) 二聚体细胞毒素 SG3199 组成。ADCT-601是由ADC Therapeutics开发,DAR值为2。当ADCT-601与表达AXL蛋白的细胞结合后,ADCT-601会内化并释放PBD,PBD会进一步进入细胞核与DNA结合。ADCT-601的临床前研究表明,在体内,ADCT-601在多种人类癌症异种移植小鼠模型中表现出显著且持久的抗肿瘤活性[8]。2019年ESMO会议上,ADC Therapeutics公布了ADCT-601 I期初步临床结果:安全性方面,13名患者接受了50‒150 µg/kg Q3W治疗,包括3名50 µg/kg、6名100 µg/kg、4名150 µg/kg。其中1名接受100 µg/kg 治疗的患者出现3级血尿的剂量限制性毒性,所有受试者都出现了治疗引起的不良事件(TEAE),其中有7名受试者出现了≥3级TEAE。ADC Therapeutics已于2020年末宣布ADCT-601临床试验中止。但据Clinical trial数据显示,针对于ADCT-601,ADC Therapeutics在2022年又启用的一项临床试验CT05389462,不同于之前终止的CT03700294,CT05389462的主要目的是确定ADCT-601的2期推荐剂量 (RP2D) 和/或最大耐受剂量 (MTD),从而来验证ADCT-601单一疗法和与吉西他滨联合疗法的安全性和耐受性。此项临床试验正处于招募状态,目前并没有相关数据展示。
Mecbotamab vedotin,亦称为BA-3011,是美国圣地亚哥的生物技术公司BioAtla经条件性激活技术(conditionally active biologics,CAB)平台设计的AXL受体靶向抗体偶联药物。其抗体部分通过CAB改造后,能选择性靶向于肿瘤组织的AXL受体,连接微观抑制剂类药物MMAE,DAR值为4。 今年1月公布的NSCLC二期临床中期分析结果显示,BA3011单药治疗的10例患者中有4例响应,ORR为40%。BA3011+Opdivo联合治疗的8例患者中,仅1例PR,ORR为13%。数据一出,BioAtla股价大跌46%。
3.2 CAR-T&抗体
CCT301-38 AXL,亦称为CCT301-38,由exumabio(原F1 Oncology)公司开发的一款针对AXL的CAR-T 产品。CCT301-38 AXL使用 F1 Oncology开发的第三代悬浮慢病毒系统和专门的T细胞封闭细胞处理系统进行处理。目前的最高临床阶段为Phase II,针对的适应症为肾细胞癌何季节性过敏性鼻炎。
3.3 抗体
Tilvestamab,亦称为BGB-149,是由Bergenbio开发的一种完全人源化的AXL阻断抗体,主要结合AXL胞外的IgG1结构,继而阻断GAS6与AXL的结合。Tilvestamab在AML、NSCLC、胰腺癌和肾癌模型中表现出抗肿瘤活性。目前,正在针对卵巢癌开展一项I期临床试验。
4、缔码AXL靶点产品助力新药研发
缔码是一家专注于提供可成药靶点临床前研发产品和服务的生物技术公司,拥有创新型功能膜蛋白开发、单B细胞先导抗体发现、抗体工程改造与功能验证平台。缔码现可提供AXL靶点全系列产品与服务,产品涵盖多种属活性蛋白、流式验证单抗及参照抗体。服务涵盖人源化、亲和力成熟、PTM风险位点去除。另外,为了加速AXL靶点药物研发,缔码还针对AXL制备了B细胞种子库,最快20天可完成先导抗体分子筛选。
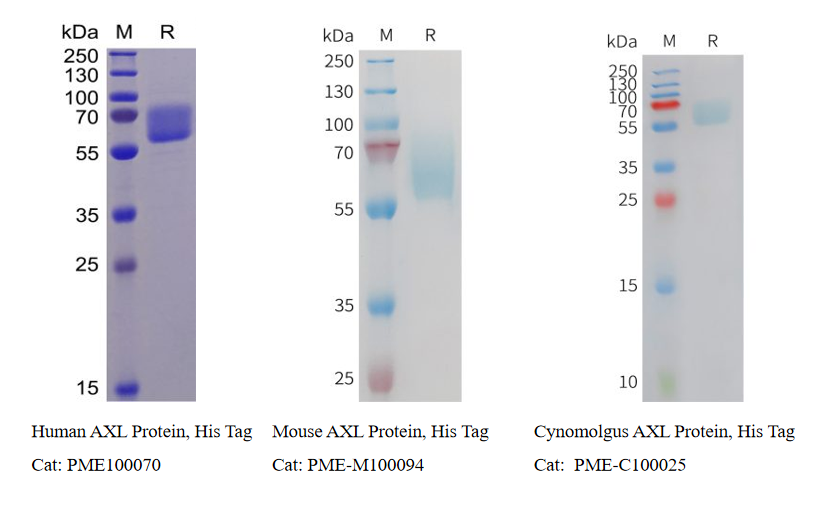
- 多种属重组蛋白
- 流式验证单抗
Anti-AXL antibody(DM158); Rabbit mAb (DME100158)
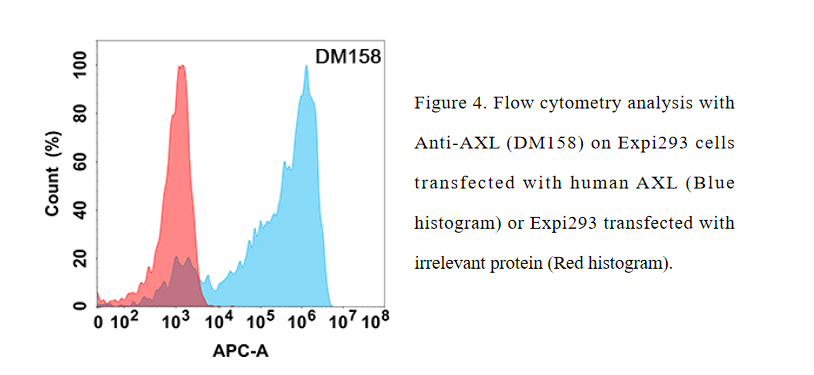
- 流式验证参照抗体
Anti-AXL(mecbotamab biosimilar) mAb ( BME100175)
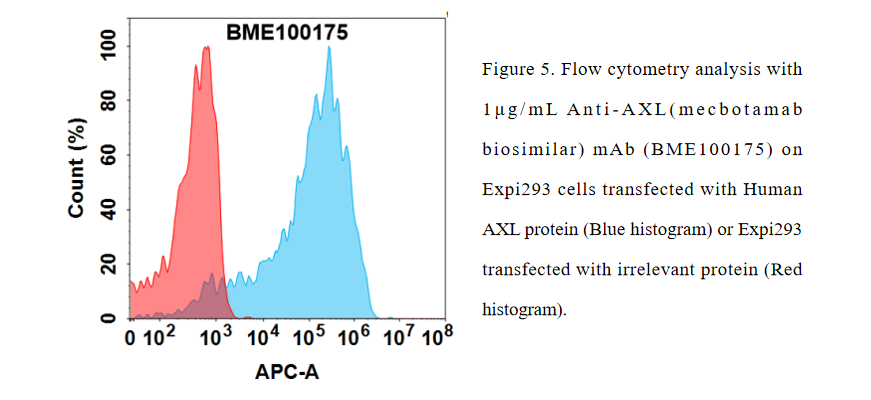
- 产品列表
| 产品类型 | 货号 | 产品名称 |
| 重组蛋白 | PME100533 | Human AXL Protein, mFc Tag |
| 重组蛋白 | PME100070 | Human AXL Protein, His Tag |
| 重组蛋白 | PME100532 | Human AXL Protein, hFc Tag |
| 重组蛋白 | PME-M100094 | Mouse AXL Protein, His Tag |
| 重组蛋白 | PME-C100025 | Cynomolgus AXL Protein, His Tag |
| FC验证抗体 | DME100158 | Anti-AXL antibody(DM158); Rabbit mAb |
| IHC验证抗体 | DMC100158 | Anti-AXL antibody(2G9), IgG1 Chimeric mAb |
| WB验证抗体 | DMC100868 | Anti-AXL antibody(1F2), IgG1 Chimeric mAb |
| 参照抗体 | BME100175 | Anti-AXL(mecbotamab biosimilar) mAb |
| 参照抗体 | BME100033 | Anti-AXL (enapotamab biosimilar) mAb |
| 生物素标记抗体 | BME100175B | Biotinylated Anti-AXL(mecbotamab biosimilar) mAb |
| 生物素标记抗体 | BME100033B | Biotinylated Anti-AXL (enapotamab biosimilar) mAb |
| 生物素标记抗体 | DMC100868B | Biotinylated Anti-AXL antibody(1F2), IgG1 Chimeric mAb |
| 生物素标记抗体 | DMC100158B | Biotinylated Anti-AXL antibody(2G9), IgG1 Chimeric mAb |
| 生物素标记抗体 | DME100158B | Biotinylated Anti-AXL antibody(DM158); Rabbit mAb |
参考文献:
[1]Liu E, Hjelle B, Bishop JM. Transforming genes in chronic myelogenous leukemia. Proc Natl Acad Sci U S A. 1988 Mar;85(6):1952-6.[2]O’Bryan JP, Frye RA, Cogswell PC, Neubauer A, Kitch B, Prokop C, Espinosa R 3rd, Le Beau MM, Earp HS, Liu ET. axl, a transforming gene isolated from primary human myeloid leukemia cells, encodes a novel receptor tyrosine kinase. Mol Cell Biol. 1991 Oct;11(10):5016-31.
[3]Tang Y, Zang H, Wen Q, Fan S. AXL in cancer: a modulator of drug resistance and therapeutic target. J Exp Clin Cancer Res. 2023 Jun 16;42(1):148.
[4]Zhu C, Wei Y, Wei X. AXL receptor tyrosine kinase as a promising anti-cancer approach: functions, molecular mechanisms and clinical applications. Mol Cancer. 2019 Nov 4;18(1):153.
[5]Uhlén M, Fagerberg L, Hallström BM, et al. Tissue-based map of the human proteome. Science. 2015 Jan 23;347(6220):1260419.
[6]olavito SA. AXL as a Target in Breast Cancer Therapy. J Oncol. 2020 Feb 14;2020:5291952.
[7]Koopman LA, Terp MG, Zom GG, et al. Enapotamab vedotin, an AXL-specific antibody-drug conjugate, shows preclinical antitumor activity in non-small cell lung cancer. JCI Insight. 2019 Nov 1;4(21):e128199.
[8]Zammarchi F, Havenith KE, Chivers S, et al. Preclinical Development of ADCT-601, a Novel Pyrrolobenzodiazepine Dimer-based Antibody-drug Conjugate Targeting AXL-expressing Cancers. Mol Cancer Ther. 2022 Apr 1;21(4):582-593.