在肿瘤免疫治疗中,一方面,我们可以通过靶向肿瘤细胞上的相应的免疫检查点,阻止癌细胞的免疫逃逸(比如PD-1、CTLA-4等),另一方面,也可增强免疫细胞对癌细胞的攻击力,本期的主角4-1BB就属于这一类,它是一种重要的共刺激分子,是T细胞活化的重要信号。
4-1BB概述
4-1BB(也称为CD137) 是一种可诱导的共刺激受体,是细胞表面糖蛋白,属于肿瘤坏死因子受体(TNFR)家族的跨膜分子,由肿瘤坏死因子受体超家族成员9(TNFRSF9)基因编码。
4-1BB主要表达在活化的CD4+和CD8+T细胞及自然杀伤细胞(NK细胞),在调节性T细胞上组成型表达。此外,4-1BB也表达在活化的巨噬细胞、B细胞和树突状细胞上。
4-1BB Ligand是4-1BB的配体,它主要表达于活化的抗原呈递细胞(APC),如树突状细胞(DC细胞)、B细胞、单核细胞、吞噬细胞等。
4-1BB和细胞免疫
众所周知,T细胞的活化是免疫应答的核心,T细胞的完全激活和增殖需要需要两种不同信号:1第一信号来自T细胞表达的TCR识别MHC/抗原肽复合物,传递抗原特异性识别信号;2
第二信号由APC的共刺激分子提供,为非特异性协同刺激信号。比如CD28:B7,4-1BB:4-1BBL等。
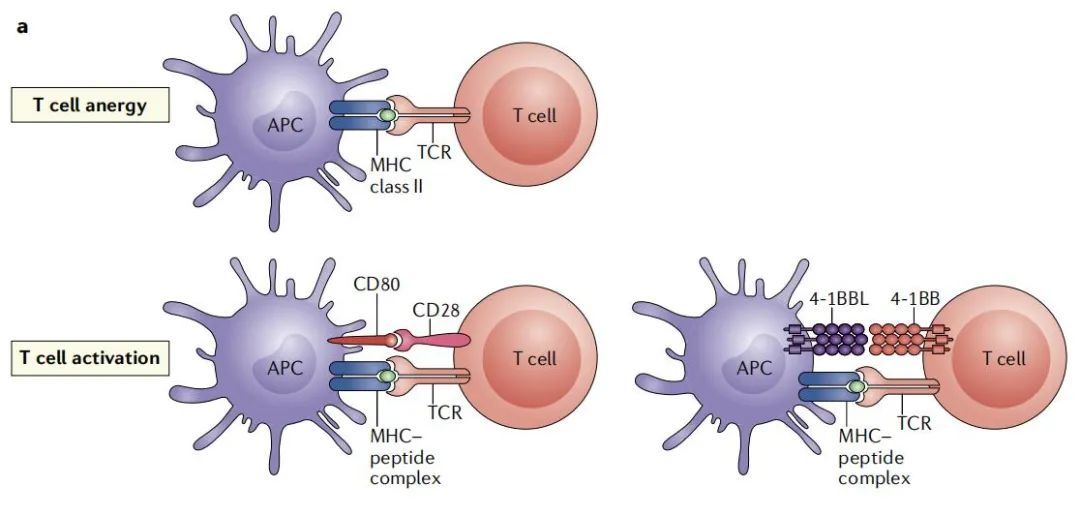
(数据来源:Cappell Kathryn M, Nat Rev Clin Oncol, 2021)[1]
4-1BB作为T细胞共刺激分子,是T细胞表面一种重要的激活型免疫检查点分子。
在体外,4-1BB信号通过上调细胞存活基因来促进T细胞的增殖和活化,同时,诱导单核细胞、树突状细胞等活化,促进细胞因子的分泌,并抑制活化诱导的细胞凋亡(Activation induced cell death,AICD)。
4-1BB信号通路
4-1BB的信号转导依赖于TRAFS蛋白。
4-1BB聚集并招募TRAF1和TRAF2形成异源三聚体。TRAF2可以与ASK1相互作用并激活ASK1。ASK1可以激活下游信号级联,包括JNK/SAPK和P38 MAPK。
通过c-Jun N末端激酶(JNK)途径,细胞外信号调节激酶(ERK)途径,以及通过β-catenin和AKT途径加强信号转导,并通过转录因子NF-κB调节4-1BB信号,促使细胞因子的产生和分泌。NF-κB的激活还通过增加抗凋亡基因bcl-XL和bfl-l的表达来促进CD8+ T淋巴细胞的存活。
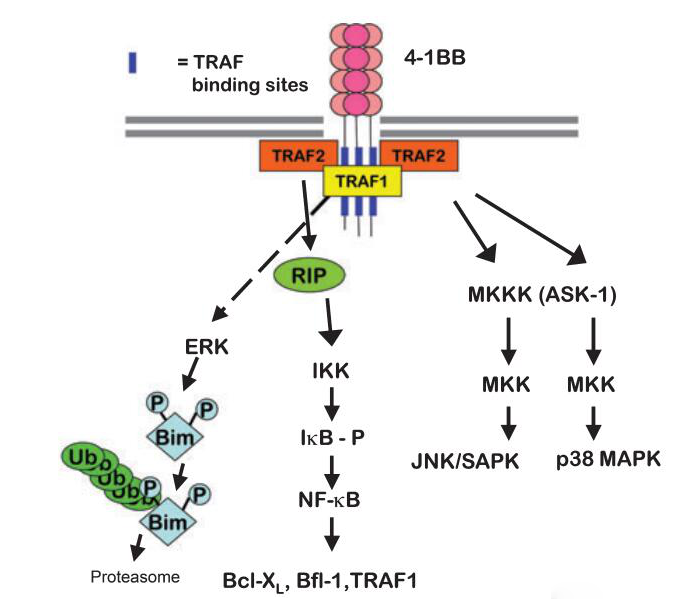
(数据来源:Chao W et al. Immunological Reviews, 2009)[2]
4-1BB与肿瘤免疫治疗
4-1BB & CAR-T
4-1BB作为共刺激因子结构域(co-stimulatory domains,CD)被广泛用于CAR-T细胞治疗。
CAR-T(嵌合抗原受体T)细胞,具有针对癌细胞的定向特异性,是一种很有前景的治疗癌症的方法。目前全球已有6款CAR-T产品上市。4-1BB广泛应用于CAR-T产品的结构设计,诺华的Kymriah的共刺激结构域是4-1BB。作为CAR-T细胞的胞内共刺激结构域,4-1BB可促进CAR-T在体内的存活和延长留存时间。
4-1BB 激活型抗体
利用配体4-1BBL或激活型4-1BB单抗激活4-1BB,可刺激T细胞和抗原提呈细胞增殖并分泌细胞因子,提高机体的抗肿瘤免疫应答水平。开发靶向4-1BB的单克隆抗体或双特异性抗体是肿瘤免疫治疗的有效手段。
抗4-1BB单抗发挥的免疫调节作用如下:
T细胞:抗4-1BB单抗诱导T细胞增殖和细胞因子分泌(A)。针对4-1BB和肿瘤抗原(如HER2)的双特异性抗体可以使免疫效应细胞近距离靶向肿瘤细胞,促进肿瘤细胞溶解(D)。2
NK细胞:在NK细胞上,4-1BB的刺激可增强ADCC(B)。3
DC细胞和巨噬细胞:激动性抗4-1BB单克隆抗体也能刺激DCs和巨噬细胞诱导抗肿瘤免疫反应,且4-1BB在肿瘤相关血管内皮中表达(C)。

(数据来源:Chester Cariad et al. Blood, 2018)[3]
单克隆抗体
目前已经有多种4-1BB激活型抗体进入临床研究阶段,包括百时美施贵宝公司(Bristol-Myers Squibb)的urelumab抗体和辉瑞公司(Pfizer)的utomilumab抗体,这些抗体单独或与其它肿瘤治疗方法联合使用,能够显著提高肿瘤治疗效率。
ADG106—-天演药业
ADG106是靶向4-1BB独特表位的激动型全人源单克隆抗体,它以一种天然的类似配体的方式激活4-1BB,阻断4-1BB配体的反向信号传导,并通过Fc受体进行有效交联。
ADG106正在进行1b/2a期临床试验,用于晚期或转移性实体瘤和/或复发/难治性非霍奇金淋巴瘤患者。
LVGN6051—-礼进生物
LVGN6051是礼进生物开发的一款靶向4-1BB的人源化单克隆激活性抗体。LVGN6051有选择性地在肿瘤微环境中局部激活4-1BB,减少正常组织免疫副反应。目前,LVGN6051正在开展多项单药或与PD-1抑制剂帕博利珠单抗联合用药的1期临床试验。
QL1806注射液—-齐鲁制药
QL1806是齐鲁美国子公司QLSF Biotherapeutics 研发的一款4-1BB人源化抗体(专利号:WO2020142624),临床前研究显示其在小鼠肿瘤中具有抗肿瘤活性。
但是激动型4-1BB抗体也存在一定的副作用。用药后4-1BB的广泛表达导致机体T细胞的过度激活,从而带来潜在的肝毒性和全身免疫反应的风险。
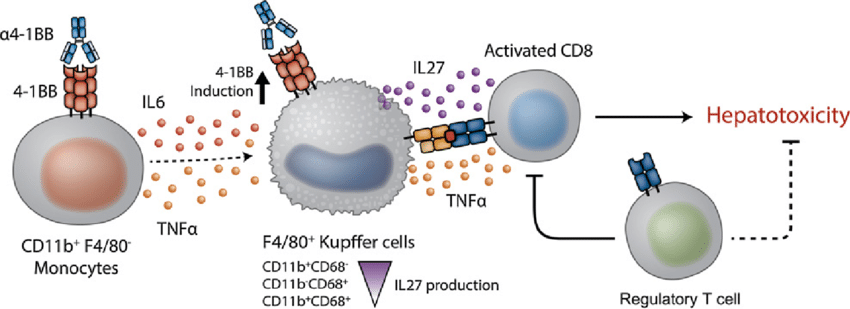
(数据来源:Bartkowiak Todd et al. Clin Cancer Res, 2018) [4]
如何确保4-1BB单一疗法的最大疗效,同时避免肝毒性?目前主要的策略如下:
瘤内(IT)给药:使肿瘤微环境中的淋巴细胞有效活化,可以有效控制用药剂量,从而减轻这类产品剂量依赖的肝脏毒性。
蛋白水解活化抗体:将掩蔽结合肽序列与单抗连接,当被肿瘤相关蛋白酶切割,其抗原结合位点暴露,这使得抗体只有在肿瘤微环境中才发挥功能,进而避免肝脏毒性。3
无Fc段设计:研究发现4-1BB单抗的肿瘤外毒性与其Fc段有关。因此,设计一种不含Fc段的肿瘤靶向4-1BB新型抗体,有望解决毒性问题。4
双特异性抗体:靶向肿瘤抗原或肿瘤基质成分的4-1BB双特异性抗体,可使诱导的T细胞激活局限于表达靶抗原的组织,从而可减轻系统毒性。在小鼠模型中,靶向CD137和肿瘤相关抗原EGFR的第一个双特异性结构体显示了疗效和增强的免疫功能,且没有明显的肝脏副作用。这种方法的局限性在于,只能对表达肿瘤相关抗原的肿瘤有效。
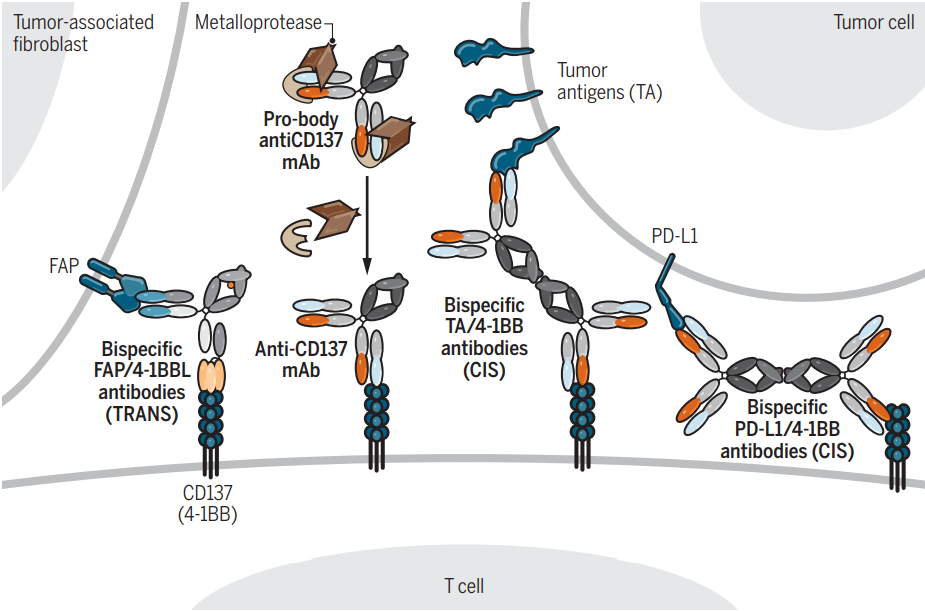
(数据来源:Sanmamed Miguel F et al. Sci Transl Med, 2019)[5]
目前,许多药企针对4-1BB靶点开发了双特异性抗体,部分企业还布局了四特异性抗体。4-1BB双特异性抗体
TJ-CD4B—天境生物
TJ-CD4B(又称ABL111),是由天境生物与韩国ABL Bio双方合作开发的靶CLDN18.2和4-1BB的双特异性抗体,已经获FDA批准开展临床研究。
TJ-CD4B具有独特4-1BB结合表位,使其仅在与Claudin 18.2结合时才会激活T细胞。TJ-CD4B的这一特性既增强了抗肿瘤免疫力,也降低了因4-1BB广泛表达而过度激活T细胞引起的肝毒性风险和降低全身免疫反应风险。
TJ-L14B—天境生物
TJ-L14B是天境生物另一款创新双抗产品,同时靶向PD-L1和4-1BB,通过阻断PD-L1信号并刺激4-1BB信号,激活T细胞产生抗肿瘤协同作用。临床前研究表明,在给药剂量相同的前提下,TJ-L14B的抗肿瘤活性既优于PD-L1抗体或4-1BB抗体的单药或联合治疗又非常持久。天境生物已于2021年4月在美国启动了TJ-L14B用于治疗局部晚期或转移性实体瘤的1期临床试验(NCT04762641)。
PM1003—普米斯生物
PM1003是一款靶向PD-L1和4-1BB的双特异性抗体,根据药审中心CDE官网公示,普米斯生物的PM1003注射液的临床试验申请获批,拟用于治疗晚期恶性实体瘤。
ATG-101—德琪医药
ATG-101是一种新型PD-L1/4-1BB双特异性抗体,拟用于治疗血液系统恶性肿瘤及实体瘤。目前,ATG-101正在转移性/晚期实体瘤和成熟B细胞非霍奇金淋巴瘤患者中,开展首次人体1期试验。
PE0116注射液—怀越生物
LBL-024—维立志博
PD-L1/4-1BB双抗。
HBM7008—和铂医药
B7H4/4-1BB新型双特异性抗体。
ES101—科望医药
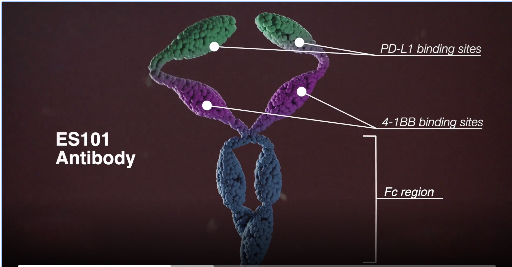
ES101最初由Inhibrx公司开发,科望医药引进其大中华区权益。ES101是一个靶向PD-L1/4-1BB的四价双特异性抗体,包含4个结合域,其中两个靶向PD-L1,另外两个靶向4-1BB。
ES101与肿瘤细胞表面的PD-L1结合,可以解除PD-1/PD-L1介导的免疫检查点抑制效应;另一方面ES101也可以结合T细胞表面的4-1BB,但是只有当ES101结合了PD-L1之后,4-1BB结合域才有可能驱动4-1BB分子在T细胞表面的聚集,这就使得4-1BB介导的免疫激活效应集中于肿瘤附近的T细胞,有效降低了潜在的脱靶毒性。
ES101目前处于2期临床试验阶段。
(数据来源:科望生物医药科技有限公司官网)[6]4-1BB四特异性抗体
除了双特异性抗体,部分企业还布局了四特异性抗体。比如百利药业的产品GNC-038、GNC-039、GNC-035。
GNC-038是百利药业GNC(Guidance navigation and control)平台下首个进入临床的候选药物,为靶向CD19、CD3、PD-L1和4-1BB的四特异性抗体。它可以激活T细胞的第一信号和第二信号,通过抗CD19、PD-L1结构域靶向并杀伤肿瘤细胞。目前GNC-038处于临床1期试验。
GNC-039将通过同时结合EGFRvIII、PDL1、CD3、41BB四个靶点,激发机体形成特异性肿瘤免疫杀伤,穿透血脑屏障、克服肿瘤靶点异质性表达、逆转抑制性的免疫微环境,从而实现肿瘤的消除。该抗体在复发/难治性或转移性实体瘤患者中的研究目前处于临床1期。
GNC-035可同时结合ROR1、PDL1、CD3、4-1BB四个靶点,激发机体形成特异性肿瘤靶向免疫杀伤,外周激活T细胞浸润肿瘤并长期维持对肿瘤细胞的杀伤、克服肿瘤靶点异质性表达、逆转抑制性的免疫微环境,从而实现肿瘤的消除。
联合用药和双特异性抗体的设计是4-1BB抗体很大的发展趋势。
| 产品类型 | 产品货号 | 产品名称 |
| 重组蛋白 | PME100011 | Human 4-1BB Protein, mFc-His Tag |
| PME100502 | Human 4-1BB Protein, His tag | |
| PME-M100007 | Mouse 4-1BB Protein, hFc Tag | |
| PME-C100023 | Cynomolgus 4-1BB Protein, hFc Tag | |
| FC验证抗体 | DME100067 | Anti-4-1BB antibody(DM67); Rabbit mAb |
| DME100066 | Anti-4-1BB antibody(DM66); Rabbit mAb | |
| 参照抗体 | BME100037 | Anti-4-1BB (utomilumab biosimilar) mAb |
| 生物素标记抗体 | DME100067B | Biotinylated Anti-41BB antibody(DM67); Rabbit mAb |
| DME100066B | Biotinylated Anti-41BB antibody(DM66); Rabbit mAb | |
| BME100037B | Biotinylated Anti-4-1BB (utomilumab biosimilar) mAb |
参考资料:
[1] Cappell Kathryn M, Kochenderfer James N, A comparison of chimeric antigen receptors containing CD28 versus 4-1BB costimulatory domains.[J] .Nat Rev Clin Oncol, 2021, undefined: undefined[2] Chao W, Lin G, Mcpherson A J, et al. Immune regulation by 4-1BB and 4-1BBL: complexities and challenges[J]. Immunological Reviews, 2009, 229(1).[3] Chester Cariad, Sanmamed Miguel F, Wang Jun et al. Immunotherapy targeting 4-1BB: mechanistic rationale, clinical results, and future strategies.[J] .Blood, 2018, 131: 49-57.[4] Bartkowiak Todd, Jaiswal Ashvin R, Ager Casey R et al. Activation of 4-1BB on Liver Myeloid Cells Triggers Hepatitis via an Interleukin-27-Dependent Pathway.[J] .Clin Cancer Res, 2018, 24: 1138-1151.[5] Sanmamed Miguel F, Etxeberría Iñaki, Otano Itziar et al. Twists and turns to translating 4-1BB cancer immunotherapy.[J] .Sci Transl Med, 2019, 11: undefined.[6] 科望生物医药科技有限公司官网https://www.elpiscience.com/cn/