GPRC5D是一种G蛋白偶联孤儿受体。GPRC5D在正常组织表达有限,但在多发性骨髓瘤(MM)细胞中独立于BCMA特异性高表达。这一表达特性,使得GPRC5D成为继BCMA后又一极具潜力的多发性骨髓瘤治疗靶点。在刚结束的2023年底65届美国血液协会(ASH)年会上,公布了多款GPRC5D靶点生物药临床试验结果,这里我们重点展示了GPRC5D靶点双抗和CAR-T细胞疗法的临床及临床前研究进展。
1、双特异性抗体
1.1 Talquetamab
TALVEY™(talquetamab-tgvs)是由强生研发的一种针对GPRC5D x CD3的双特异性抗体,已于2023年获得美国FDA批准,用于治疗至少经历了四种先前疗法的RRMM患者,也是目前所有GPRC5D靶向药中临床进展最快的一款抗体药。2023 美国血液学年会(ASH)上,强生公布了多项TALVEY™的临床研究数据。
- 3377 Updated Results of Talquetamab, a GPRC5D×CD3 Bispecific Antibody, in Patients with Relapsed/Refractory Multiple Myeloma with Prior Exposure to T-Cell Redirecting Therapies: Results of the Phase 1/2 MonumenTAL-1 Study
之前 1/2 期MonumenTAL-1 研究(NCT03399799/NCT04634552)的结果表明,Talquetamab对复发/难治性多发性骨髓瘤(RRMM)患者有深度且持久的缓解,其中288名未接受过 T 细胞重定向疗法(TCR)治疗患者的总体缓解率 (ORR) 超过 71%,51例接受过TCR治疗患者的总缓解率(ORR)为65%。最新更新的结果共纳入70例先前接受过TCR治疗的RRMM患者,结果显示,Talquetamab在既往接受过BCMA CAR-T细胞治疗患者中的ORR为72.9%,中位持续缓解时间(mDOR)>1年;在既往接受过BCMA BsAb治疗患者中的ORR为52.2%;在既往接受过BCMA ADC和TCR治疗患者中的ORR为75% [1]。
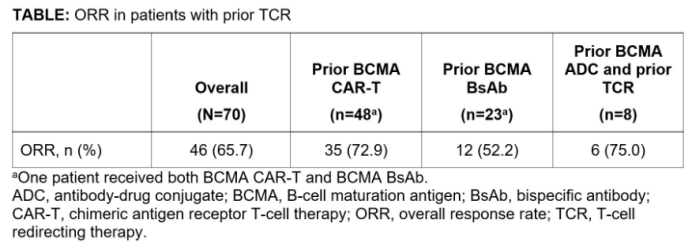
Table 1. ORR in patients with prior TCR数据来源 [1]
关于1/2 期MonumenTAL-1 研究(NCT03399799/NCT04634552),此次会议上还汇报了R/RMM患者中Talquetamab较少频率/剂量的有效性和安全性(编号1010);RRMM患者中Talquetamab的耐药和复发机制(编号1933)。
- 1014 Talquetamab + Pomalidomide in Patients with Relapsed/Refractory Multiple Myeloma: Safety and Preliminary Efficacy Results from the Phase 1b MonumenTAL-2 Study
MonumenTAL-2(NCT05050097)是一项Talquetamab与抗骨髓瘤药物泊马度胺(pom)联合治疗MM患者的多组1b期研究。此次强生展示了MonumenTAL-2研究中Talquetamab+pom的初步疗效和安全性结果。结果显示,Talquetamab联合泊马度胺可使RRMM患者或接受过两种及以上治疗(LOT)患者获得快速、深度缓解。QW和Q2W队列的ORR分别为86.7%和83.3%,完全缓解(CR)率分别为60%和44.4%,非常好的部分缓解率(VGPR)分别为86.7%和77.8%。QW队列至首次缓解的中位时间为1.0个月,Q2W队列为1.3个月。两个队列的6月PFS率分别为93.3%和88.9% [2]。
1.2 Lbl-034
4672 Lbl-034, a Highly Differentiated T-Cell Engaging Bispecific Antibody Targeting GPRC5D for the Treatment of Relapsed or Refractory Multiple Myeloma
Lbl-034是由南京维立志博生物自主研发的一种靶向GPRC5D和CD3的人源化IgG1亚型非对称型的双特异性抗体,旨在对GPRC5D表达肿瘤细胞执行T细胞介导的靶向攻击。独特的分子设计使LBL-034可以较高的结合力特异性结合到表达GPRC5D的肿瘤细胞上,并同时减少对T细胞的非特异性激活的风险,从而增强了抗肿瘤疗效和降低了潜在的免疫毒性风险。维立志博在2023 ASH公布的临床前结果显示:Lbl-034可诱导GPRC5D产生强效的T细胞依赖性细胞杀伤作用,提高活化标志物的表达和细胞因子释放,增强抗肿瘤活性,同时降低CD3诱导的CRS风险,具有良好的抗肿瘤活性。
目前Lbl-034已获得FDA和NMPA临床试验批准。现正在中国开展I期临床NCT06049290,这是一项单臂、开放标签、多中心、剂量递增且扩展的首次I/II 期临床研究,旨在验证Lbl-034在RRMM患者中的安全性和耐受性,确定其I/II期临床试验的推荐剂量,并评估其治疗效果。
1.3 RG6234
1948 Co-Expression of GPRC5D, FcRH5 and BCMA Suggests That Targeting More Than One Cell Surface Marker May be a Viable Strategy in Relapsed/Refractory Multiple Myeloma (RRMM): Biomarker Results from the Phase I Study of Forimtamig, a GPRC5DxCD3 Bispecific Antibody
RG6234,又称Forimtamig,是罗氏研发的一种新型2:1结构的靶向GPRC5DxCD3双特异性单克隆抗体,包含两个与靶点结合的蛋白域和一个与CD3结合的蛋白域。目前临床研发阶段为Phase I。
罗氏在2023 ASH会议上公布了Forimtamig I期临床研究中在生物标志物上探索结果,GPRC5D和FcRH5在75.4%的MM 浆细胞 (MMPC)上共表达;其次是共表达GPRC5D和BCMA(中位数31.9%)或BCMA和FcRH5(中位数25.3%)。在大多数患者中很少观察到双阴性和三阴性MMPCs (在所有分析的患者中,只有0.5-6%的MMPC仅表达三个靶标中的一个或不表达)。GPRC5D、FcRH5 和 BCMA 的共表达表明,靶向多个 MM 表面标志物可能会导致对单个肿瘤细胞的双重/三次打击,以促进快速和深度的肿瘤清除,并在RRMM 患者中实现持久的反应。
2、三特异性抗体
456 Characterization of JNJ-79635322, a Novel BCMAxGPRC5DxCD3 T-Cell Redirecting Trispecific Antibody, for the Treatment of Multiple Myeloma
JNJ-79635322是强生开发的一种靶向BCMA/GPRC5D/CD3的三特异性抗体,由抗CD3结合域、抗BCMA结合域和抗GPRC5D结合域组成。该三特异性抗体利用对浆细胞进行双重抗原识别,有可能通过双靶点亲和力增强与肿瘤细胞结合,从而有效清除恶性克隆群,并防止肿瘤抗原丢失介导的耐药性。目前全球临床最高研发阶段为Phase I。
强生在2023 ASH上公布了JNJ-79635322的临床前试验结果,结果表明,JNJ-79635322可在体外多种骨髓瘤细胞系内诱导强大的细胞毒性,同时伴有T细胞激活。值得注意的是,JNJ-79635322能够有效地消除双靶点(BCMA和GPRC5D)和单靶点(BCMA或GPRC5D)表达细胞。此外,在体内,JNJ-79635322在小鼠MM细胞异种移植模型(表达单靶点的克隆H929 细胞)和两种肿瘤消退模型(RPMI 8226 和 MM.1S 细胞)中表现出有效的抗肿瘤活性 [3]。目前,JNJ-79635322治疗骨髓瘤患者的剂量递增1期研究正在进行中(NCT05652335)。
3、CAR-T细胞疗法
3.1 BMS-986393
219 BMS-986393 (CC-95266), a G Protein–Coupled Receptor Class C Group 5 Member D (GPRC5D)–Targeted Chimeric Antigen Receptor (CAR) T-Cell Therapy for Relapsed/Refractory Multiple Myeloma (RRMM): Updated Results from a Phase 1 Study
BMS-986393(CC-95266)是百时美施贵宝(“BMS”)研发的靶向GPRC5D的自体CAR-T细胞疗法。目前临床最高研究阶段phase I。BMS在2023 ASH会议上分享了一项首次人体、多中心、开放标签I期研究,评估BMS-986393在先前接受过三种及以上疗法的RRMM患者中的作用。本研究的主要目的是确定BMS-986393的安全性、耐受性和最大耐受剂量和/或推荐的Ⅱ期剂量(RP2D),次要目的包括初步疗效的评估。
公布的结果显示,在可评估疗效的患者中,不同剂量的ORR为86%(55/64),在既往接受过BCMA靶向疗法(包括CAR-T细胞)的患者中,ORR为75%(21/28),CR为38%(24/64)。在既往未接受BCMA靶向治疗的患者中,ORR为94.4%(34/36),CR为38.9%(14/36)。所有治疗患者的中位随访时间为5.9个月(范围,0.0-24.0)。其中150×106 CAR-T细胞剂量组 (推荐的二期剂量),ORR为91.3%,CR为43.5%。
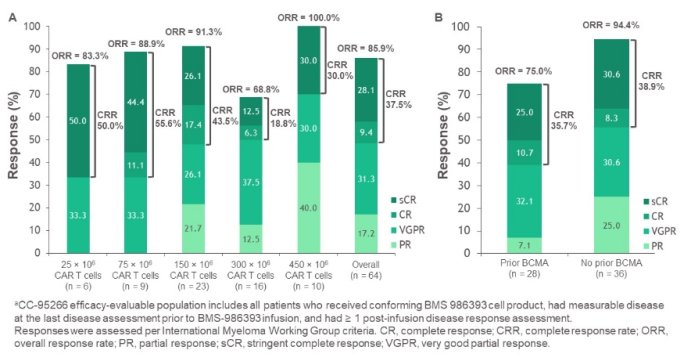
Figure 1. Best overall response (A) by dose level and (B) according to prior BCMA treatment (efficacy-evaluable analysis set) 数据来源 [4]
在这项首次人体研究中,BMS-986393在所有测试的剂量水平下都表现出可控的安全性和深度持久缓解。CRS和ICANS型神经毒性大多级别较低,在300×106和450×106 CAR-T细胞剂量下,≥3级事件增加。少数患者发生了1/2级的脱靶TRAEs。
3.2 缔码生物,广州百暨基因和云南920医院GPRC5D CAR T Cell Therapy
3472 Safety and Efficacy of GPRC5D CAR T Cell Therapy in Relapsed/Refractory Multiple Myeloma Patients
这篇关于GPRC5D CAR T 细胞治疗的IIT临床报道,是由缔码生物联合广州百暨基因在中国人民解放军联勤保障部队第920医院,中国医学科学院血液学研究所两地开展GPRC5D CAR-T临床研究。此款疗法是一款第二代 GPRC5D CAR-T细胞疗法,由结合GPRC5D的scFv(源自人源化兔单克隆抗体)、4-1BB共刺激结构域和CD3ze信号结构域组成。当前全球临床最高研发阶段为:探索性临床IIT研究。缔码生物CEO马东晖博士在2023 ASH会议上展示了部分临床试验(NCT05739188)结果。
NCT05739188是一项单中心、开放标签、单臂的I期研究,旨在评估抗GPRC5D CAR-T 细胞疗法在RRMM受试者中的有效性和安全性。迄今为止,此项试验总共入组了7名RR MM患者,其中包括3名既往接受过BCMA CAR-T 治疗的患者。所有患者均在2023年2月7日至2023年11月13日期间接受自体CAR T细胞输注并进行临床评估。总体缓解率为85.7%(6/7),其中5例完全缓解(CR),1例部分缓解(PR),1例无缓解(NR)。该NR患者此前未表现出对BCMA CAR-T 疗法有反应,用FACS分析证实其肿瘤细胞上不存在BCMA和GPRC5D。就目前的结果而言,GPRC5D CAR T细胞疗法在RR MM患者中表现出良好的临床疗效和可耐受的安全性。现在这项临床试验仍然在继续招募患者……
4、缔码GPRC5D靶点产品助力新药研发
缔码是一家专注于提供可成药靶点临床前研发产品和服务的生物技术公司,拥有创新型功能膜蛋白开发、单B细胞先导抗体发现、抗体工程改造与功能验证平台。缔码现可提供GPRC5D靶点全系列产品与服务,产品涵盖多种属活性蛋白、流式验证单抗及参照抗体。服务涵盖人源化、亲和力成熟、PTM风险位点去除。为助力GPRC5D靶点药物研发,缔码现针对流式推荐抗体Anti-GPRC5D antibody(DM91); Rabbit mAb (DME100091)和免疫组化推荐抗体Anti-GPRC5D antibody(DM61); Rabbit mAb (DME100061)试用装申请活动。
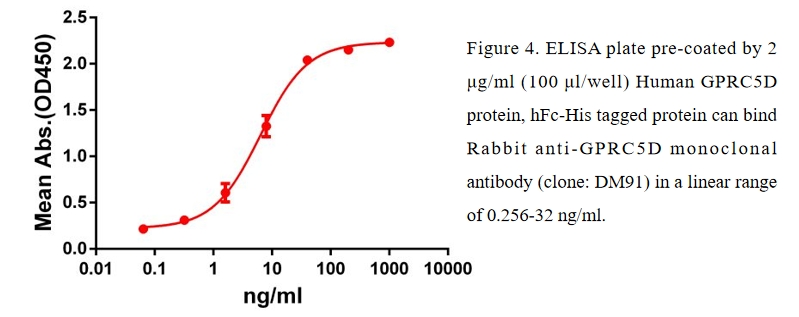
ELISA验证

FC验证
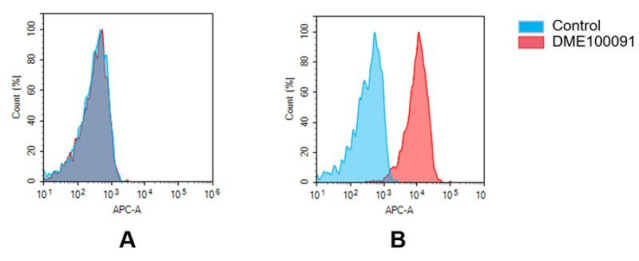
Figure 3. Flow cytometry analysis of antigen binding of rabbit anti-human GPRC5D mAb (DME100091). (A) DME100091 does not bind to Jurkat cells that do not express GPRC5D. (B) A clear peak shift of DME100091 was seen compared to the control when incubated with GPRC5D-expressing MM.1S cells, indicating strong binding of DME100091 to GPRC5D. Antibodies were incubated at 5 µg/mL.
ELISA验证
IHC验证
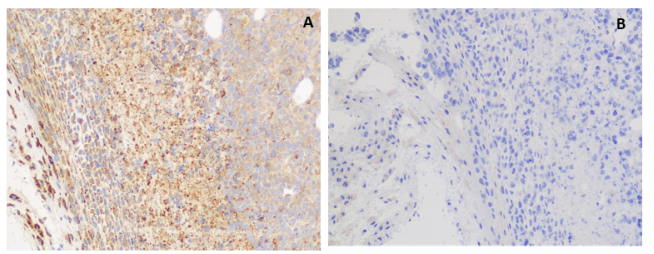
Figure 5. IHC staining of H929 cells A. with rabbit anti-GPRC5D mAb (Cat# DME100061) at 5.9 ug/ml. B. with another anti-GPRC5D mAb (Cat# DME100090) at 8.8 ug/ml. DME100061 can specifically react with GPRC5D in IHC application.
- 试用装申请
- 活动时间:2024年1月1日-1月31日
- 活动对象:终端客户
- 活动说明:该活动不与其他优惠同享,本活动最终解释权归缔码生物科技有限公司所有。
- 其他GPRC5D产品试用:缔码生物已自研多种GPRC5D相关抗体产品,若您需要PE标记或Biotin标记的产品,可在表单中填写您的需求,提交后1个工作日内会有缔码工作人员与您联系。
- 申请方式:扫描下方二维码填写申请表单。提交后会有缔码工作人员与您联系,以便确认相关信息。

参考文献:
[1]Andrzej J Jakubowiak,et al. 2023 ASH. Poster 3377.
[2]Jeffrey V Matous, et al. 2023 ASH. Oral 1014.
[3]Ram Pillarisetti, et al. 2023 ASH. Oral 456.
[4]Susan Bal, MD, et al. 2023 ASH. Oral 219.

