癌胚蛋白5T4又称Wnt 激活抑制因子 1(WAIF1)、滋养层细胞糖蛋白(TPBG),是一种存在于胚胎滋养层细胞中的糖蛋白。因在成人正常组织中表达受限,但在许多实体瘤恶性肿瘤中高表达而被选为实体瘤靶点。据Clinical trial数据统计,目前5T4在研药物差不多9种,临床管线也才近20条,但其药物类型比较多样,涉及肿瘤疫苗、融合蛋白、ADC、双抗、CAR-NK。其中,肿瘤疫苗(Trovax)和融合蛋白(Naptumomab estafenatox)进展最快,目前最高研发状态处于临床II期。解锁多条生物药类型的5T4究竟是什么?目前各类型药物的进展又是如何?一文带您了解全部详情。
1、5T4的结构及表达
5T4是由TPBG基因编码的脊椎动物特异性单次跨膜蛋白,编码蛋白的基因位于染色体6q14-15上。5T4蛋白是N端高度糖基化的跨膜蛋白,首次在人胎盘组织中发现 [1]。人类5T4全长蛋白的分子量约为72kDa,蛋白序列保守,由420个氨基酸组成。5T4蛋白在胞外结构域中包含一个细胞外区、一个跨膜区(356-376aa)和一个胞内区(如Figure 1所示)[2][3]。细胞外区含有多个富含亮氨酸的重复序列 (LRR)和7个N糖基化位点。LRR区参与蛋白质间互作,糖基化位点结构多样,能够防止蛋白质水解。胞内区含有PDZ结合基序(Ser-Asp-Val),该结合基序可以与TIP-2/GIPC互相作用。TIP-2/GIPC是一种与位于细胞附近的囊泡相关的细胞质蛋白膜。与TIP-2/GIPC互相作用可参与细胞迁移和黏附信号转导过程的调控。

Figure 1. The structure of 5T4 [4]
5T4在正常成人组织中很少表达,但广泛表达于胚胎发育期的各滋养层细胞和大多数常见肿瘤中。在约80%的肾癌、乳腺癌、结肠癌、前列腺癌和卵巢癌中高表达。
2、5T4的信号通路
由于5T4在正常组织和癌症组织中的差异化表达,所以5T4可作为具有潜在治疗价值的肿瘤治疗靶点。但目前对该分子在肿瘤中的作用机制了解仍然很少。但现存研究表明5T4可能是通过Wnt信号通路、上皮-间质转化和CXCR4/CXCL12通路发挥作用。
2.1 5T4与Wnt信号通路
Wnt信号通路是胚胎发育的关键通路,对个体的正常发育、细胞内稳态和再生至关重要。Wnt有两条途径,Wnt/β-catenin经典途径和非经典途径。Wnt/β-catenin经典途径的关键是粘附连接相关蛋白β-catenin向细胞核的积累和易位。而Wnt非经典途径又称平面细胞极性(PCP)途径,是Wnt配体与Frizzled受体或其共受体结合从而引发级联反应。Wnt信号通路在正常成熟细胞中处于未激活状态,但在肿瘤细胞中活性增强。
研究已证实,5T4会干扰 Wnt/β-catenin 信号传导并同时激活非经典Wnt通路,对Wnt信号通路具有双重调节。5T4与Wnt共受体LRP6结合并抑制其与Wnt受体的内吞,从而阻断Wnt/β-catenin经典信号通路,继而抑制细胞黏附和细胞骨架的形成,促进肿瘤迁移和扩撒。此外,5T4通过活化DKK1来激活非经典Wnt通路,促进细胞迁移和浸润 [5]。

Figure 2. Model of Waif1a function as modifier of Wnt signaling pathways [5]
2.2 上皮细胞-间充质转化
上皮间质转化(EMT)指上皮细胞向间质细胞转化的现象,它赋予细胞转移和入侵的能力,与恶性肿瘤的发生发展、侵袭及转移有着密切的关系。有研究表明5T4被是小鼠和人胚胎干细胞早期分化的标志物,该过程涉及多个EMT经典特征,包括E-cadherin向N-cadherin的转换、E-cadherin抑制分子(如Snail和Slug蛋白)的上调及基质金属蛋白酶(MMP-2和MMP-9)活性增强 [6] [7] [8]。
2.3 CXCR4/CXCL12通路
CXCL12和CXCR4表达都与许多肿瘤的发生有关。而且有研究表明CXCR4的表达有助于癌症扩散到CXCL12高表达的组织中,比如肺、肝、淋巴结和骨髓 [9] [10]。5T4被证实参与一些胚胎和肿瘤细胞表面CXCR4的功能表达,可通过CXCR4/CXCL12通路,促进肿瘤细胞的趋化转移 [11] [12]。
3、5T4的临床进展
目前全球并未有针对5T4的靶向药上市,最高的研发状态是Phase II。据Clinical trial数据统计,目前有9个药物处于临床阶段,其中有5款药物处于Phase II,4款处于Phase I(有一款在Early Phase I)。
3.1 处于II期临床的药物
Ankara-5T4 vaccine(疫苗)是由SWOG Cancer Research Network开发的癌症疫苗,针对适应症为乳腺癌,最高临床阶段为Phase II,目前关于其在临床上的效果报道较少。
TroVax(疫苗),又称为MAV-5T4,是改良版的Ankara-5T4 vaccine,由英国Oxford BioMedica公司开发的癌症疫苗。TroVax是减毒修饰牛痘病毒安卡拉,经过改造后编码人类5T4抗原,通过刺激机体产生抗5T4的免疫应答来杀伤癌细胞。目前临床上已针对多种适应症展开临床试验,涉及肠癌、前列腺癌、肾癌、卵巢癌和间皮瘤。临床上的给药方式也涉及多种,包括单药和联用。其中联用又涉及与IL-2、Nivolumab(PD-1)或GM-CSF联用。2017年发表的一项随机临床试验数据表明,在本次试验纳入的55名不可手术且在标准化疗后病情稳定的转移性结肠癌患者中,其中9名患者仅接受环磷酰胺治疗、19名患者仅接受MVA-5T4治疗及18名患者接受MVA-5T4和环磷酰胺联合用药治疗。结果显示MVA-5T4和联合治疗组的5T4特异性抗体免疫反应显着增强,延长患者OS/PFS(20/10.3月 vs 5.6/2.4月)[13]。
Naptumomab estafenatox(NAP)(重组蛋白)是由NeoTX Therapeutics开发的融合蛋白,由一个识别5T4的抗原结合片段(Fab)与一种金黄色葡萄球菌肠毒素A(SEA/E-120)的突变形态(estafenatox)组成。Sag部分选择性地与T细胞受体β变量 (TRBV) 7-9 结合。T细胞通过直接杀伤、分泌细胞因子清除肿瘤细胞。目前,最高研发状态为Phase II,针对的适应症为非小细胞肺癌、肾癌和胰腺癌。2016年发表的一项关于NAP与IFNα联合用药治疗肾细胞癌的临床II/III期试验结果表明,这项II/III期研究未达到其主要终点。NAP+IFN患者的中位OS/PFS为17.1/5.8个月,而单独接受IFN的患者为 17.5/5.8 个月,NAP联合IFNα用药的安全性在可接受范围内 [14]。
ALG.APV-527(双抗)是由Aptevo Therapeutics和Alligator Bioscience AB联合开发的双特异性抗体,同时靶向4-1BB和5T4,拟开发适应症为实体瘤。目前最高的研发状态为Phase II。ALG.APV-527临床前数据显示,ALG.APV-527具有在不刺激身体其他部位免疫系统的情况下,选择性加强肿瘤中T细胞反应潜力。
GEN1044(双抗)是由Genmab和AbbVie联合开发的双特异性抗体,同时靶向人T细胞表面抗原CD3和癌胎抗原5T4,具有潜在的免疫调节和抗肿瘤活性。当前最高研发状态为Phase II,针对的适应症是实体瘤,但相关临床数据暂未披露。
3.2 处于I期临床的药物
ASN004(ADC)是由Kirilys Therapeutics公司开发的靶向癌胎抗原5T4的新型单链scFv-Fc抗体,通过Dolaflexin可裂解连接子技术偶联auristatin衍生物(AF-HPA)。ASN004目前处在临床I期,针对的适应症包括乳腺癌、非小细胞肺癌、肠癌和卵巢癌。临床前试验显示,ASN004可在多种肿瘤异种移植模型中诱导完全和持久的肿瘤消退,这些模型来源于具有广泛5T4表达水平的人肺、乳腺、宫颈和胃肿瘤细胞系 [15]。
PF-06263507(ADC)是由Pfizer开发的抗体偶联药物,由anti-5T4人源化抗体、不可剪切连接子(mc)和MMAF组成。目前处于临床I期,针对的适应症为非小细胞肺癌、乳腺癌和卵巢癌。临床前研究结果证实PF-06263507有优秀的抗肿瘤活性。但在临床I期剂量递增试验中,PF-06263507没有观察到ORR,存在眼部毒性(推测是MMAF引起的)为主的DLT。目前辉瑞已终止临床开发。
SYD1875(ADC)是由Byondis B.V.开发的一款抗体偶联药物,由anti-5T4人源化抗体、可裂解连接子和双卡霉素类似物组成。目前最高研发状态为临床I期,主要针对的适应症为实体瘤。
IBR854(CAR-NK)为英百瑞开发的CAR-raNK 细胞疗法,核心是将靶向肿瘤抗原5T4的特异性抗体通过linker与同种异体外周血来源通用现货型的NK细胞进行共价偶联。目前IBR854已获得国家药监局临床试验默示许可,是国内首个针对实体肿瘤的CAR-raNK细胞疗法,全球首创的FIC产品。目前正处在早期临床I期。
4、缔码5T4靶点产品助力新药研发
缔码是一家专注于提供可成药靶点临床前研发产品和服务的生物技术公司,拥有创新型功能膜蛋白开发、单B细胞先导抗体发现、抗体工程改造与功能验证平台。缔码现可提供5T4靶点全系列产品与服务,产品涵盖多种属活性蛋白、流式验证单抗及参照抗体。服务涵盖人源化、亲和力成熟、PTM风险位点去除。另外,为了加速5T4靶点药物研发,缔码还针对5T4制备了B细胞种子库,最快20天可完成先导抗体分子筛选。
- 多种属蛋白

- ELISA&流式验证抗体
Anti-5T4 antibody(DM139); Rabbit mAb (DME100139)

Figure 3. Validation data of Anti-5T4 antibody. Human 5T4 protein, His tagged protein can bind Rabbit anti-5T4 monoclonal antibody in a linear range of 0.1-16 ng/ml (left); 5T4 protein is highly expressed on the surface of Expi293 cell membrane (right).
- ELISA&流式验证参照抗体
Anti-5T4 reference mAb (BME100158)
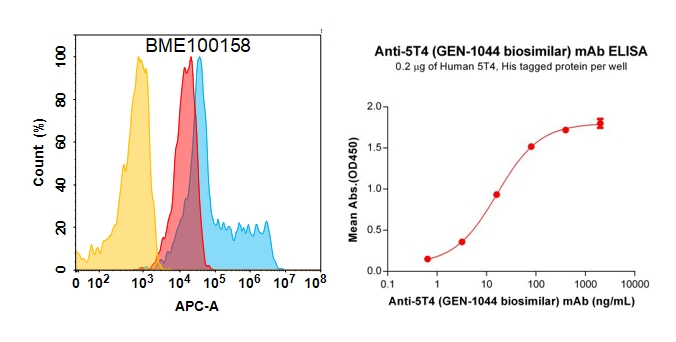
Figure 4. Validation data of Anti-5T4 reference mAb. 5T4 protein is highly expressed on the surface of Expi293 cell membrane (left); Human 5T4 Protein, His Tag (PME100123) can bind Anti-5T4 reference mAb (BME100158) in a linear range of 0.64–16 ng/mL (right).
参考文献:
[1]Hole N, Stern PL. A 72 kD trophoblast glycoprotein defined by a monoclonal antibody. Br J Cancer. 1988 Mar;57(3):239-46.
[2]Myers K.A., Rahi-Saund V., Davison M.D., et al. Isolation of a cDNA encoding 5T4 oncofetal trophoblast glycoprotein. An antigen associated with metastasis contains leucine-rich repeats. J. Biol. Chem. 1994;269:9319–9324.
[3]Zhao Y, Malinauskas T, Harlos K, et al. Structural insights into the inhibition of Wnt signaling by cancer antigen 5T4/Wnt-activated inhibitory factor 1. Structure. 2014 Apr 8;22(4):612-20.
[4]Tsuboi A. LRR-Containing Oncofetal Trophoblast Glycoprotein 5T4 Shapes Neural Circuits in Olfactory and Visual Systems. Front Mol Neurosci. 2020 Oct 28;13:581018.
[5]Kagermeier-Schenk B, Wehner D, Ozhan-Kizil G, et al. Waif1/5T4 inhibits Wnt/β-catenin signaling and activates noncanonical Wnt pathways by modifying LRP6 subcellular localization. Dev Cell. 2011 Dec 13;21(6):1129-43.
[6]Ward CM, Barrow K, Woods AM, et al. The 5T4 oncofoetal antigen is an early differentiation marker of mouse ES cells and its absence is a useful means to assess pluripotency. J Cell Sci. 2003 116(Pt 22):4533–4542
[7]Ward CM, Eastham AM, Stern PL. Cell surface 5T4 antigen is transiently upregulated during early human embryonic stem cell differentiation: effect of 5T4 phenotype on neural lineage formation. Exp Cell Res. 2006, 312(10):1713–1726
[8]Eastham AM, Spencer H, Soncin F, Ritson S, Merry CL, Stern PL et al. Epithelial-mesenchymal transition events during human embryonic stem cell differentiation. Cancer Res. 2007, 67(23):11254–11262
[9]Balkwill F. The significance of cancer cell expression of the chemokine receptor CXCR4. Semin Cancer Biol. 2004, 14(3):171–179
[10]Burger JA, Kipps TJ. CXCR4: a key receptor in the crosstalk between tumour cells and their microenvironment. Blood. 2006, 107(5):1761–1767
[11]Southgate TD, McGinn OJ, Castro FV, R et al. CXCR4 mediated chemotaxis is regulated by 5T4 oncofetal glycoprotein in mouse embryonic cells. PLoS ONE. 2010, 5(4):e9982
[12]McGinn OJ, Marinov G, Sawan S, et al. CXCL12 receptor preference, signal transduction, biological response and the expression of 5T4 oncofoetal glycoprotein. J Cell Sci. 2012, 125(Pt 22):5467–5478.
[13]Scurr M, Pembroke T, Bloom A, et al. Effect of Modified Vaccinia Ankara-5T4 and Low-Dose Cyclophosphamide on Antitumor Immunity in Metastatic Colorectal Cancer: A Randomized Clinical Trial. JAMA Oncol. 2017 Oct 12;3(10):e172579.
[14]Hawkins RE, Gore M, Shparyk Y,et al. A Randomized Phase II/III Study of Naptumomab Estafenatox + IFNα versus IFNα in Renal Cell Carcinoma: Final Analysis with Baseline Biomarker Subgroup and Trend Analysis. Clin Cancer Res. 2016 Jul 1;22(13):3172-81.
Smith RA, Zammit DJ, Damle NK, et al. ASN004, A 5T4-targeting scFv-Fc Antibody-Drug Conjugate with High Drug-to-Antibody Ratio, Induces Complete and Durable Tumor Regressions in Preclinical Models. Mol Cancer Ther. 2021 Aug;20(8):1327-1337.
