目前为止,大部分治疗性抗体药物都是从小鼠或者人源化小鼠开发出来的,小鼠仍然是开发治疗性抗体药物的首要选择。但是,随着1997 年兔单克隆抗体的融合细胞株240E-W的发现和RabMAb®平台的建立,鼠单抗的局限性被克服。近年来,考虑到兔单抗独特的优势,越来越多的生物制药企业和科研工作者开始选择兔单抗平台来开发抗体药物。
兔单抗的优势
更高的亲和力和特异性
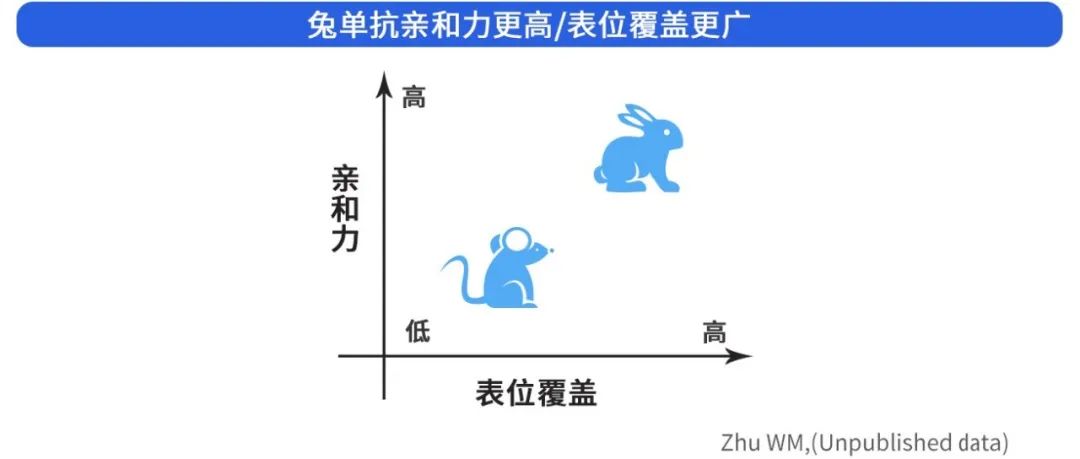
高亲和力是优质抗体的筛选指标之一。平均而言,兔单克隆抗体对靶抗原的亲和力是小鼠单克隆抗体的 10-100 倍。这得益于兔子有独特的B细胞发育过程,还有双重亲和力成熟机制,也就是基因转换和超突变。
更为多样性的免疫抗体谱/表位覆盖广
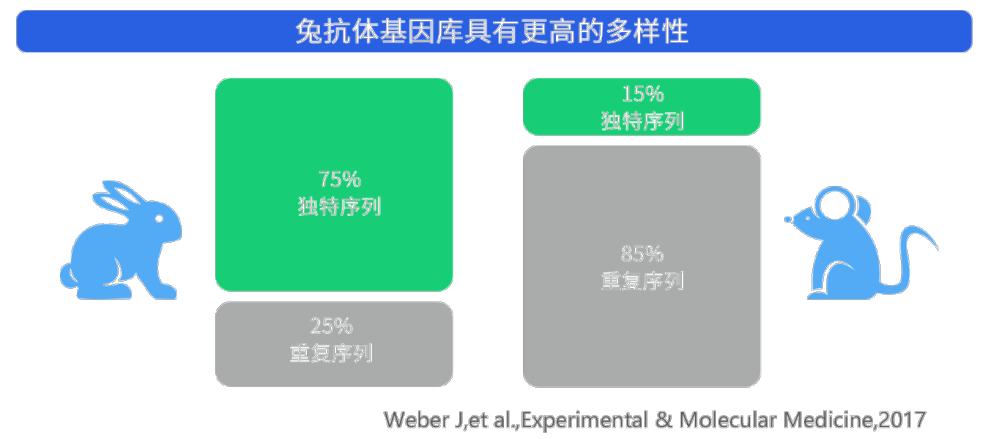
与小鼠相比,兔拥有更丰富的免疫抗体谱,这是由于兔的免疫抗体谱系产生机制除了有体细胞超突变过程,兔还有一个基因转换机制。也正因如此,兔抗甚至可以识别部分鼠抗不能识别的抗原表位。兔抗体在区分诸如表位变异(如修饰)、突变和构象变化等细微差别方面也更具优势。

针对弱免疫原性抗原的单抗开发
针对小分子和半抗原,小鼠等啮齿动物不会产生明显的免疫反应,而兔能产生好的免疫反应,因此针对弱免疫原性的抗原,兔单抗就是更好的选择。
易于人源化
兔IgG结构简单抗体亲和力高,也更容易进行人源化改造。
单个个体产生的B细胞数量更多
从兔子身上回收的B细胞数量是老鼠的50-100倍。
兔单抗因其独特的优势,在药物临床开发,伴随诊断,细胞治疗等领域得到越来越广泛的应用:
FDA获批药物
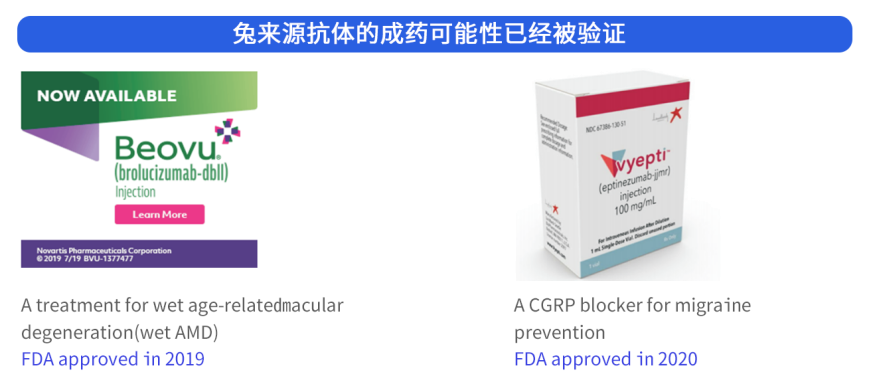
2019年4月15日,诺华的Beovu (brolucizumab) 获得了FDA的批准。它是一种靶向VEGF的兔来源通过人源化改造的治疗性单克隆抗体,用于治疗湿性年龄相关性黄斑变性(AMD)。
2020年2月21日,FDA批准了eptinezumab-jjmr (Vyepti)在成人偏头痛预防治疗中的应用,这是一款靶向降钙素基因相关肽(CGRP)的人源化抗体。
这两款兔源经过人源化后单克隆抗体的获批,证明了兔单抗的可成药性。
临床阶段的药物
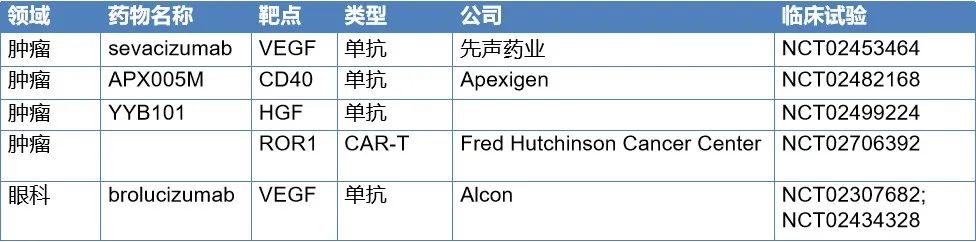
以下是目前一部分正在临床试验阶段的兔源单抗,具体如下表:
伴随诊断用途兔单抗相关产品
目前,已经有数十种兔单克隆抗体被 FDA 批准用于相关疾病的临床诊断。主要涉及肿瘤相关抗原的表达检测,包括HER2、雌激素受体、孕酮受体和PD-L1。

为帮助药企加快抗体药临床前开发的步伐,缔码生物基于单B细胞技术开发了缔码重组兔单抗开发平台,应用该平台对所有可成药靶点制备缔码单克隆抗体先导抗体分子和相应的缔码单克隆抗体B细胞种子库。药企客户可以从缔码生物直接引进先导抗体分子或从B细胞种子库快速筛选更多抗体。目前,我们围绕血液肿瘤、免疫检查点、实体瘤相关170+靶标,已开发出B细胞种子库及对应的先导抗体分子,并已完成人-兔嵌合, 其中大部分靶点的分子已完成人源化改造。